 药物所首页
药物所首页
 药物所首页
药物所首页


近日,中国科学院上海药物研究所罗成研究员团队与大连化学物理研究所王方军研究员团队合作,创新性地整合了非变性质谱(nMS)、紫外激光解离技术(UVPD)与X射线晶体学,成功揭示了弥漫性胃癌相关靶蛋白RhoA 的Y42C突变体“隐藏”动态构象,进一步发现了针对该“隐藏”构象的共价抑制剂。这一多维技术路线充分利用了紫外激光解离质谱在靶蛋白动态构象和瞬态互作测量方面的高选择性和高灵敏度优势,为靶向高动态的“不可成药”蛋白确立了全新的研究范式。
2026年3月16日,该工作以“Discovering Targetable Conformation of RhoA Mutant by Integrating Native Mass Spectrometry, Ultraviolet Photodissociation and X-Ray Diffraction”为题,发表在《美国化学会志》(Journal of the American Chemical Society)上。
Ras超家族蛋白的致病突变往往通过诱发微小且高度动态的构象变化导致生物学功能紊乱,面对这类“不可成药”靶标,传统的X射线晶体学等常规结构解析方法面临巨大挑战:往往只能捕捉到非生理状态下的静态结构,难以反映蛋白质在溶液中的关键功能构象。在本研究中,团队在研究GDP结合态RhoA Y42C突变体时,晶体学技术解析出了两种结构,Mg2+分别由Thr37或Pro36骨架羰基配位,使得真实致病分子机制陷入了“盲区”。为了突破这一技术瓶颈,研究团队利用非变性质谱(nMS)与193-nm紫外激光解离(UVPD)技术,以单残基分辨率精确绘制局部构象变化。相关结果证实Pro36配位是突变体在溶液中的主导状态,Y42C突变增强了对Mg2+的亲和力,形成“Mg2+锁定效应”。同时,UVPD揭示了Switch I区域构象改变导致关键水分子丢失,致使GTP水解能力受损;而局部疏水相互作用的破坏使Cys42附近柔性显著增加,在三维空间形成一个隐藏的新口袋(Cys42/Switch I口袋)。据此,团队筛选出共价抑制剂LC-RhoAY42Cin。该抑制剂能选择性修饰突变体Cys42位点,并呈剂量依赖性地抑制核苷酸交换。
上海药物研究所罗成团队与大连化学物理研究所王方军团队围绕如何利用大连相干光源紫外激光解离质谱开展创新药物靶标发现开展了长期合作(JACS 2023)。罗成团队在蛋白质动态调控与创新药物早期发现取得系列研究进展(Nature, 2021; Cancer Cell, 2023; Nat. Methods, 2025; Nature Commun., 2023/2025;JACS 2025;Angew Chem Int Ed Engl.2021/2025等)。王方军团队致力于发展生物大分子质谱新仪器和新方法,在大连相干光源搭建了高能紫外激光解离-串联质谱仪器,已在蛋白质及其复合物动态结构和相互作用的质谱分析中取得了系列研究进展(Nat Protoc 2023;JACS 2023/2024/2025;Anal Chem 2026)。
该工作的共同第一作者为上海药物所博士研究生吴昊哲、大连化学物理研究所刘哲益副研究员、原上海药物所蒋昊博士(现为加州大学圣地亚哥分校博士后)。该工作的通讯作者为罗成研究员与王方军研究员。本研究得到了国家蛋白质中心(上海)、上海同步辐射光源的支持,获得了国家重点研发计划、国家自然科学基金、中国科学院战略性先导科技专项等项目的资助。
全文网址:http://pubs.acs.org/doi/abs/10.1021/jacs.5c20067
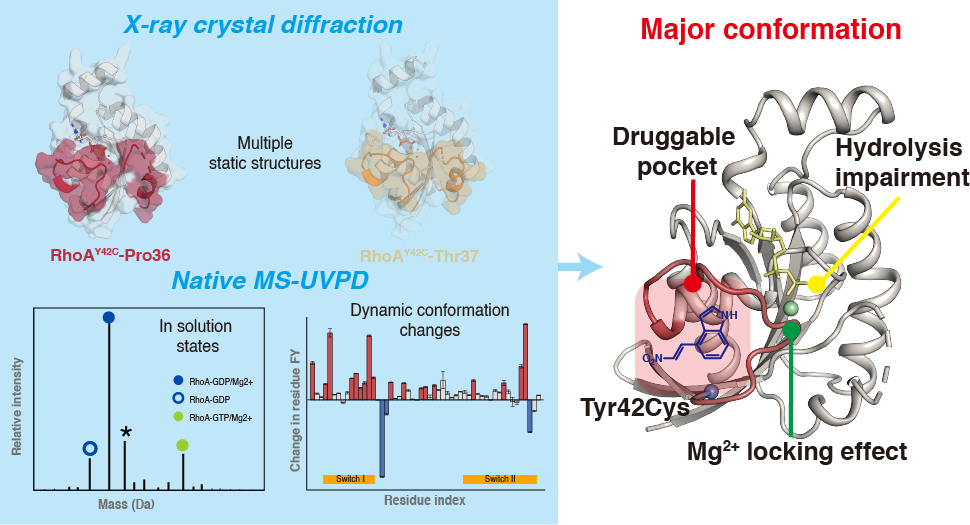
图1. native MS-UVPD解析Y42C突变动态构象变化
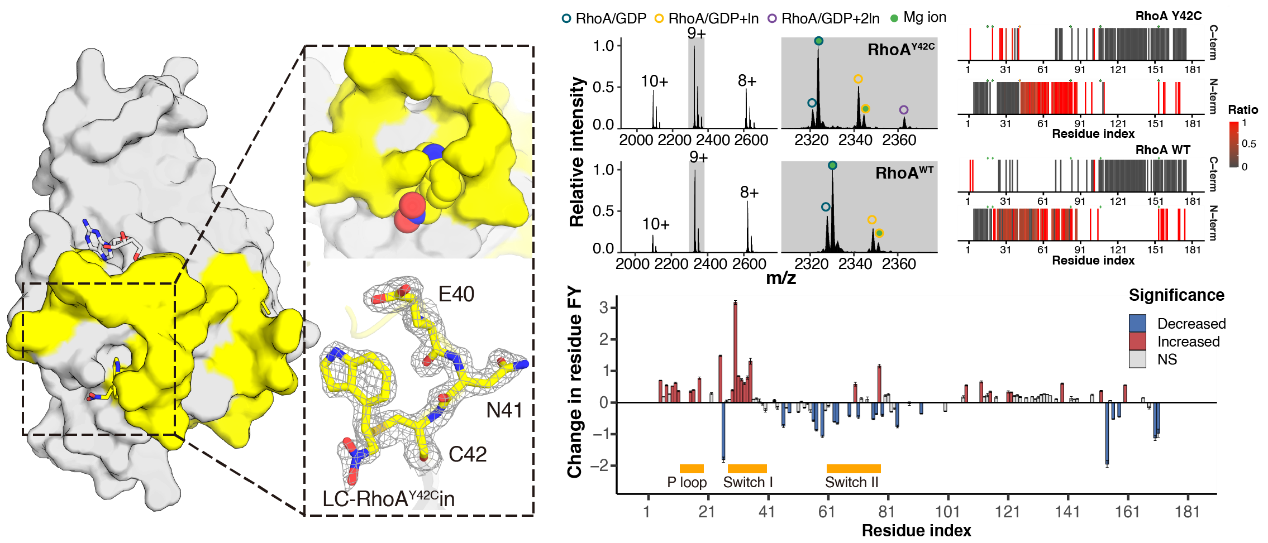
图2. 高分辨复合物晶体结构和UVPD-MS研究表明LC-RhoAY42Cin特异性结合Y42C位点
(供稿部门:罗成课题组)