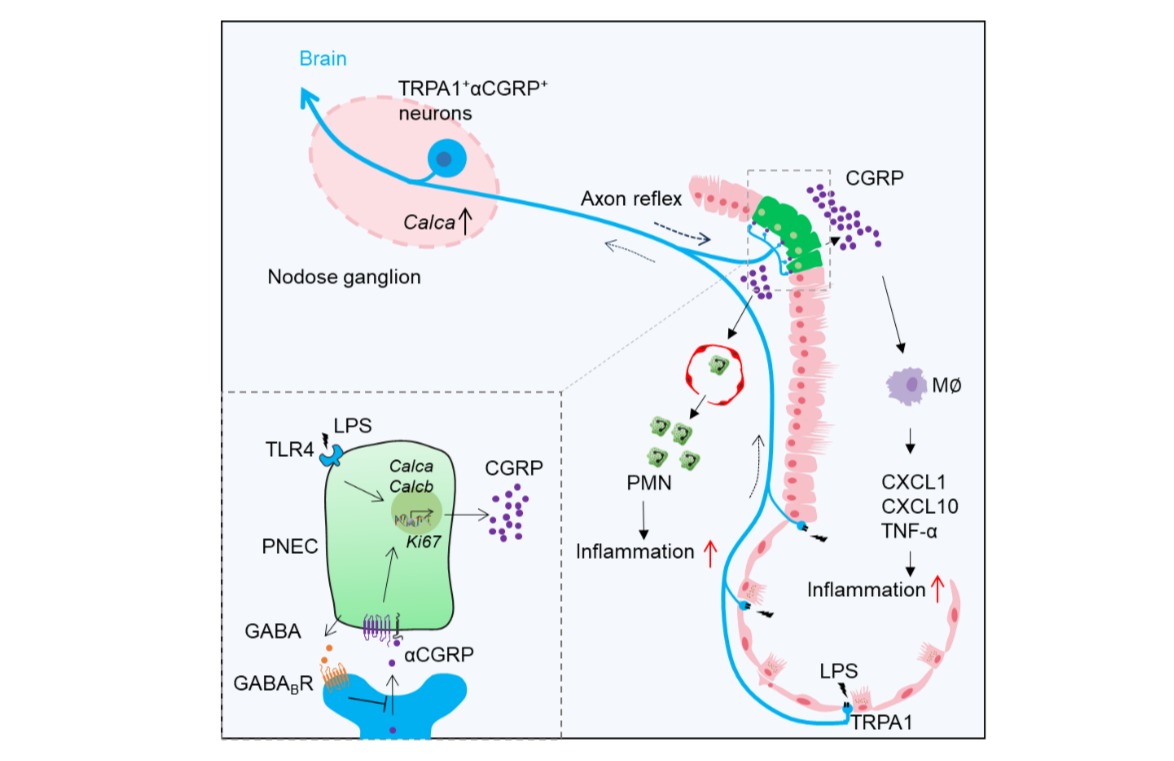
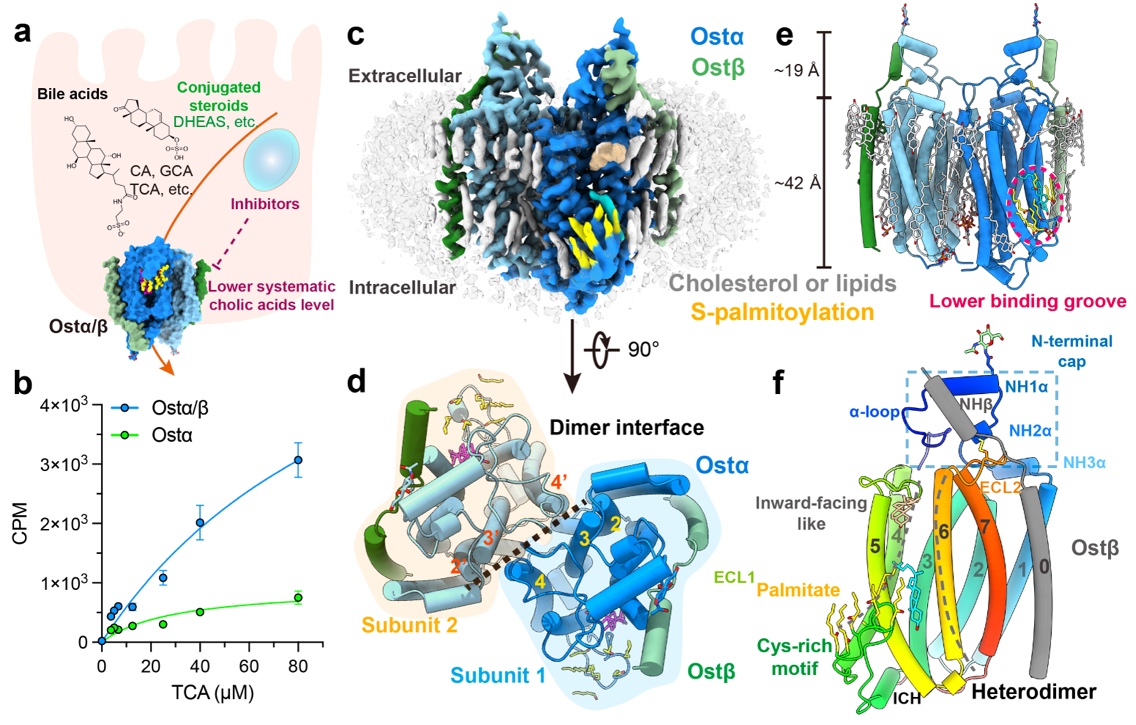
JACS | 上海药物所在复杂鞘糖脂合成方面取得进展
鞘糖脂是一类两亲性的复杂生物分子,其结构特征为亲水性糖链通过糖苷键与疏水性脂质共价连接。这类分子广泛分布于细胞和组织中,参与细胞识别、免疫逃逸、病原体感染与肿瘤转移等多种重要的生理和病理过程。然而,由于糖鞘脂固有的异质性和结构复杂性,直接从天然的样品中分离获取结构明确且数量充足的糖脂非常困难。尽管通过化学法、酶法或化学酶法能实现特定种类鞘糖脂的合成,但糖链与脂质的低偶联效率限制了化学合成法的广泛应用,而糖脂底物的低水溶性也极大阻碍了酶促反应的高效进行。目前,结构多样化的复杂鞘糖脂合成仍面临巨大挑战,进而阻碍了糖脂的生物学功能研究及相关药物的开发。
为了解决上述问题,中国科学院上海药物所李铁海课题组于2025年2月11日在Journal of the American Chemical Society上发表了题为 “Host-Guest Chemistry-Mediated Biomimetic Chemoenzymatic Synthesis of Complex Glycosphingolipids ” 的文章。该研究发展了一种“主客体化学”介导的仿生化学酶促合成策略(图1),实现了结构多样化复杂鞘糖脂的高效制备,弥补了糖科学研究中糖脂库构建技术的欠缺,为复杂糖脂的高效合成提供了新方法。
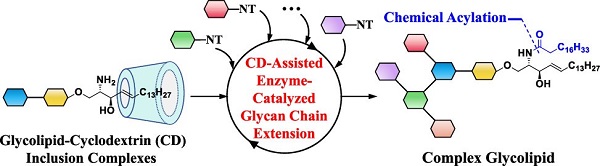
图1. 环糊精协助的仿生化学酶促合成复杂鞘糖脂
研究团队利用甲基-β-环糊精与两亲性糖基鞘氨醇自组装,促使脂肪链部分嵌入环糊精的疏水腔,糖链部分暴露于其亲水表面以进行一系列高效的酶催化反应,形成的糖脂产物能够通过C18固相萃取快速纯化。随后,通过选择性酰化反应高效引入第二条脂肪链,成功构建包含20种具有不同岩藻糖化和唾液酸化修饰的中性及酸性鞘糖脂库 (图2)。该糖脂库涵盖具有重要生物学意义的globo-、 ganglio-、 neolacto- 和 lacto-系列糖脂,为基于糖脂的免疫治疗试剂与疫苗的研究提供了物质基础。
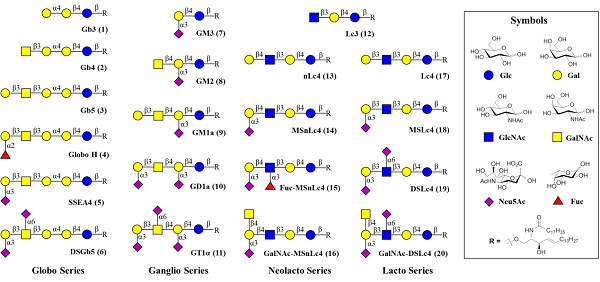
图2. 合成的结构多样化复杂鞘糖脂库
上海药物所博士研究生马源、硕士研究生刘雅亭和曹畅为共同第一作者,李铁海研究员为通讯作者。该研究获得了上海药物所文留青研究员的支持,并得到了国家自然科学基金委项目、中国科学院战略性先导科技专项、上海市科委项目和生命过程小分子调控全国重点实验室的资助。