Angew | 上海药物所发展“强支点占据-杠杆干扰”PPI先导化合物开发新策略
蛋白-蛋白相互作用(protein-protein interaction,PPI)参与信号转导、结构组装以及细胞周期调控等过程。PPI的失衡或异常可直接引发癌症、神经退行性病变及自身免疫病等一系列疾病。传统的PPI抑制剂开发受限于界面平坦、亲和力低等问题,其药物化学优化是目前研究的难点,难以快速获得高活性、高选择性的PPI先导化合物。针对上述问题,中国科学院上海药物研究所罗成及其合作团队创造性提出“强支点占据-杠杆干扰”(Fulcrum Occupancy–Leverage Perturbation,FOLP)的PPI先导化合物设计策略,将已知高亲和力片段作为“支点”(Fulcrum)稳固锚定正构口袋,再利用分子模拟技术设计“杠杆”(Leverage)伸入邻近的互作界面处潜在变构口袋,扰动互作界面,快速获得高活性PPI抑制剂。从而实现撬动PPI,最终破坏PPI的目的。相关成果于2025年8月19日以“Fulcrum Occupancy–Leverage Perturbation Strategy Enables Rapid Discovery of Potent CDK2–Cyclin A2 Interaction Inhibitors”为题在线发表于Angewandte Chemie International Edition,并被推荐为“Hot Paper”。
PPI广泛参与多种疾病的发生、发展、恶化及迁移的各个过程,并在其中发挥重要促进作用,与传统药物靶标相比,PPI界面具有开放性、动态性、广泛性等特点。针对这一关键问题,罗成课题组及其合作者长期开发化学生物学新技术、新方法,聚焦PPI新靶标发现与化学干预,取得系列原创性成果:基于虚拟筛选技术,发现了首个靶向铜离子伴侣蛋白Atox1和CCS二聚体PPI的小分子抑制剂(Nature Chem 2015)和SPOP/PTEN的PPI先导化合物(Cancer Cell 2016);靶向EED-EZH2互作界面,获得其首个PPI抑制剂(J Med Chem 2014, J Med Chem 2021); 靶向LC3/P62,设计了国际上首个进入临床的LC3候选药物(Angew Chem 2021, J Med Chem 2024);基于CDK12-DDB1-Cyclin K复合物调控,提出“双位点”稳定互作,获得其新型分子胶(Nat Commun 2024);发现天然产物丹酚酸B可增强PRDX1-DOK3相互作用,缓解类风湿性关节炎(APSB 2025)等。
该研究针对PPI抑制剂设计耗时低效、难以快速获得高活性先导化合物的问题,提出FOLP新策略并以CDK2-Cyclin A2为模型完成其概念验证。首先,通过分子动力学模拟和基于深度学习的口袋发现工具PocketMiner,确定CDK2的A-loop位置存在潜在的变构口袋。进而,以泛CDK抑制剂AT7519为“支点”往A-loop口袋延伸杠杆,快速合成并筛选出nM级PPI抑制剂LC-K2CAin-3(IC50 = 32.1 nM)。X射线衍射复合物晶体结构和氢氘交换质谱数据证实该化合物稳定A-loop,将CDK2锁定在不利于与Cyclin A2结合的构象,从而瓦解其蛋白-蛋白相互作用。最终,LC-K2CAin-3在CDK2高表达的黑色素瘤细胞中通过选择性破坏CDK2与Cyclin A2相互作用,进而诱导G2/M期阻滞与细胞凋亡,确证其具备抗肿瘤的潜力。
综上所述,该策略不仅可为PPI领域研究提供新的概念和方法,该工作流程和理论依据将有助于针对其它PPI调控剂的未来开发。
上海药物所罗成研究员、周兵研究员、陈奕研究员和华东师范大学陈示洁研究员为该论文共同通讯作者。上海药物所孙葛博士、浙江大学/上海药物所联合培养博士池帅帅、原上海药物所李佳城博士(现为芝加哥大学博士后),上海药物所徐盼博士、林婷婷博士和博士后陈超为该论文的共同第一作者。该研究得到了国家蛋白质中心(上海)、上海同步辐射光源的支持,获得了国家重点研发计划、国家自然科学基金等项目的资助。
全文链接:https://onlinelibrary.wiley.com/doi/10.1002/ange.202513542
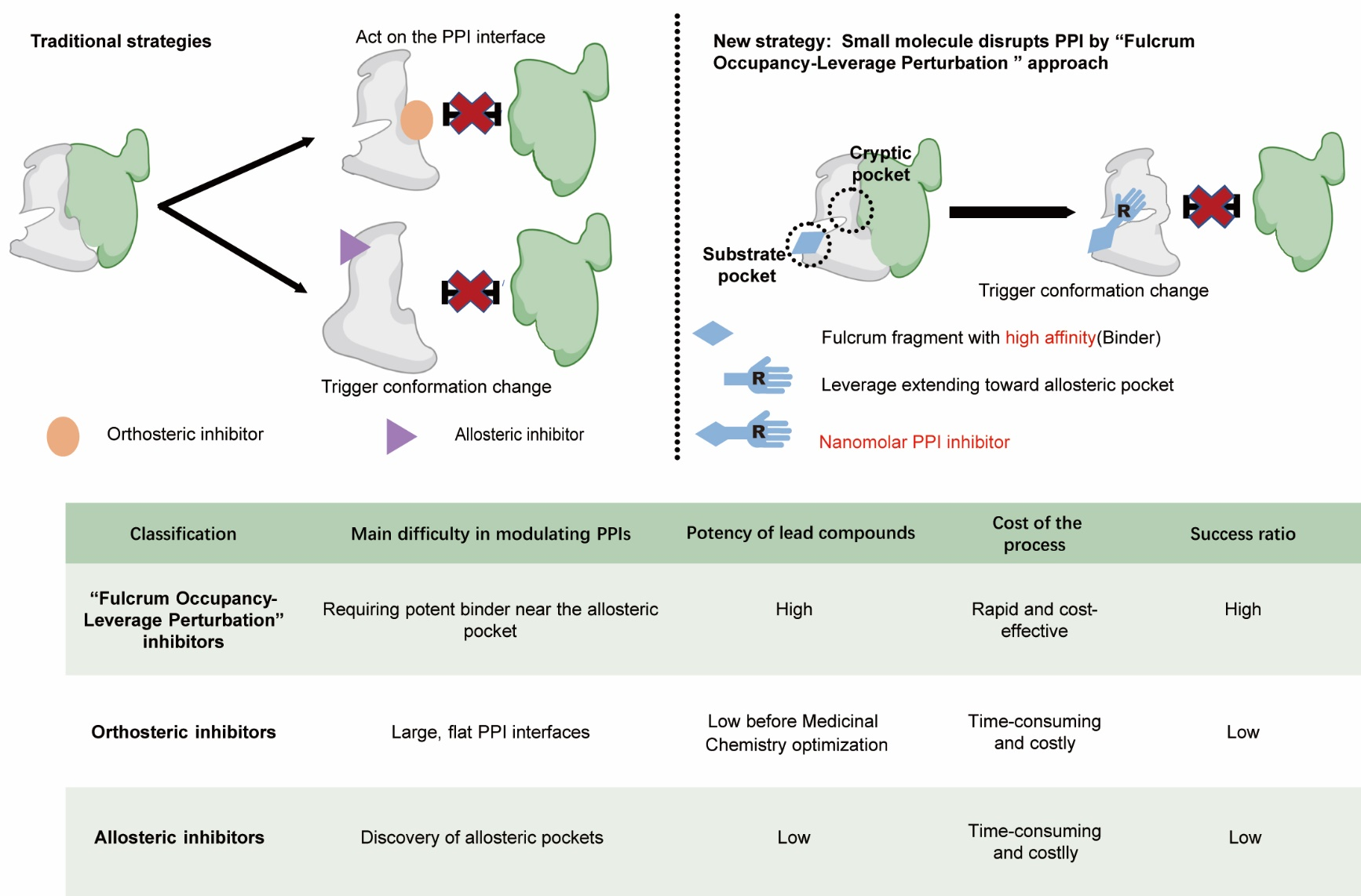
图1. 传统PPI设计策略与FOLP策略的优劣比较
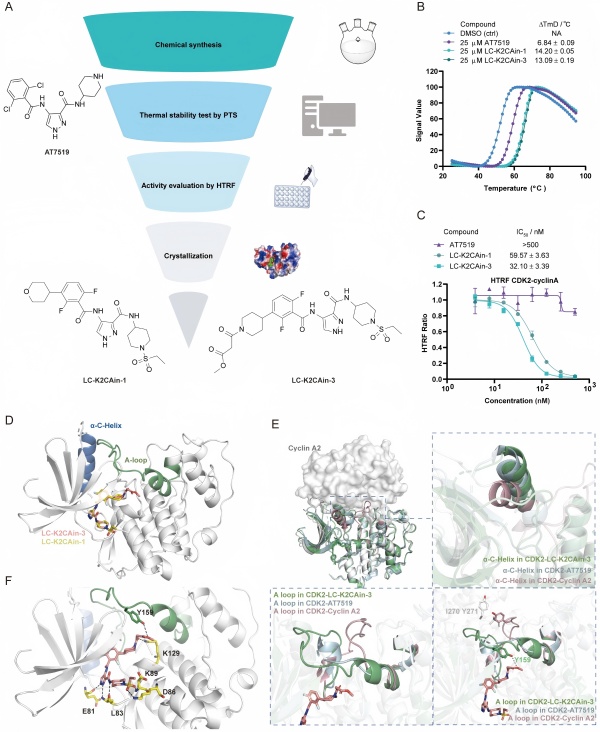
图2. CDK2-Cyclin A2互作抑制剂LC-K2CAin-3的活性表征与结构基础解析
(供稿部门:罗成课题组)