Angew | 上海药物所开发基于酶促C(sp3)–H氧官能化技术不对称合成羟基酸
羟基可以显著改变小分子的理化特性,对生物活性至关重要,是活性天然产物和药物中最普遍的官能团之一。不对称C(sp3)–H直接氧官能化策略近几年在有机合成中备受青睐,但往往依赖于高温条件或者是过渡金属催化。由于不同C(sp3)–H的解离能相差较少,选择性不对称C(sp3)–H直接氧官能化的合成工具还有待丰富。因此,开发具有高区域选择性、高立体选择性、高效的C(sp3)–H直接氧官能化技术具有重要意义。
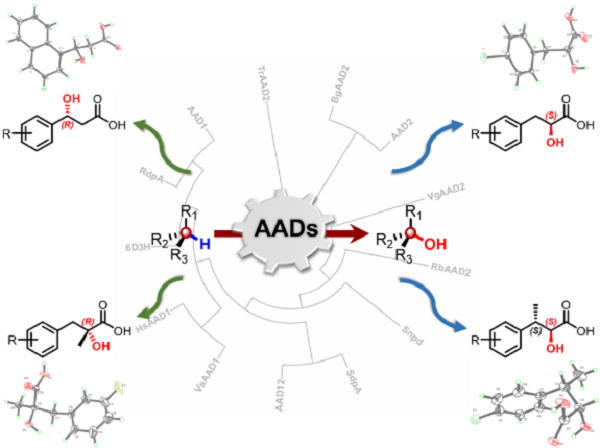
针对上述问题,中国科学院上海药物研究所廖苍松团队联合郑明月团队及广州中医药大学吴杰伟副研究员,基于对非血红素铁依赖双加氧酶的挖掘,以苯丙酸类底物的C(sp3)–H直接氧官能化策略完成了α-、β-羟基酸的酶法不对称合成(图一)。该研究成果于2023年6月20日以“Versatile Biocatalytic C(sp3)–H Oxyfunctionalization for Site-selective and Stereodivergent Synthesis of α- and β- Hydroxy Acids”为题在线发表于Angewandte Chemie International Edition。
研究人员受芳氧乙酸除草剂的天然降解酶(AADs)启发,基于对非血红素铁依赖双加氧酶催化机制的理解,在本研究中设计了不对称C(sp3)–H直接氧官能化的羟基酸合成反应。科研人员利用分子对接评估潜在的结合可能性,对接结果表明R-AADs和S-AADs具有不同的位点选择性和立体选择性。鉴于自然界已经进化出多种AAD变体,团队利用酶相似性工具(EFI-EST)挖掘AAD,然后应用序列相似性网络(SSN)来可视化天然AAD之间的同源关系。
研究人员选取并表达了13种天然AADs酶与34种不同取代苯丙酸类化合物进行反应筛选,其中R-AADs选择性对苯丙酸类化合物的的Cβ–H进行氧官能化,生成R构型的羟基酸;S-AADs选择性对苯丙酸类化合物的的Cα–H进行氧官能化,生成S构型的羟基酸,实验结果与最初的分子对接结果相吻合。不同的酶变体对不同取代基的底物分子具有互补的应用范围,研究人员进行了制备合成及产物表征。此外,研究人员考察了α-、β-有甲基取代苯丙酸类化合物的反应性,结果显示α-甲基苯丙酸可以与R-AADs反应,生成含有季碳手性中心的α-羟基酸。S-AAD对 (R)-β-甲基苯丙酸的Cα位展现出氧官能化反应活性,合成具有两个相邻立体中心的(αS,βS)-α-羟基-β-甲基苯丙酸。最后,研究人员利用全细胞催化分别实现了四类产物的克级规模制备。
在本项研究中,上海药物所团队开发了一种C(sp3)–H对映选择性氧官能化的酶催化技术,以合成不同类型的手性羟基酸类化合物。天然酶变体的多样性赋予了反应多样化的位点和对映选择性,以及优异的底物范围。该技术为合成和药物化学提供有价值的手性砌块,为针对特定底物C(sp3)–H氧官能化的酶工程改造奠定了基础。
上海药物所廖苍松研究员、郑明月研究员以及广州中医药大学吴杰伟副研究员为论文共同通讯作者。上海药物所毛迎乐助理研究员、上海药物所-广州中医药大学联合培养研究生张伟杰、上海药物所博士后付尊蕴为论文共同第一作者。巴塞尔大学Florian P. Seebeck教授参与了课题的讨论。该论文得到国家自然科学基金、上海市自然科学基金、临港实验室等项目的资助。
图1:酶促不对称羟基酸合成技术
(供稿部门:廖苍松课题组)