JACS | 上海药物所开发甲硫氨酸选择性脱硫编辑新策略
2025年5月5日,中国科学院上海药物研究所黄蔚课题组于Journal of the American Chemical Society发表了题为Bioinspired Methionine-Selective Desulfurization Editing of Peptides via the Photocatalysis Strategy的研究论文。该研究受酶催化独特的断键模式所启发,发展了一种光催化甲硫氨酸选择性脱硫策略,可以精准地对多肽进行编辑,拓展了多肽修饰的化学空间,同时促进了硫鎓化学在可见光催化反应中的应用。
S-腺苷甲硫氨酸(SAM)作为一类经典的辅酶因子,参与SAM依赖型甲基转移酶和SAM自由基酶等催化的各类反应,介导生命体中各式各样的化学转化过程。一般而言,SAM自由基酶通过引发SAM分子中S−C(5′) 键的均裂,产生高度活泼的5′-脱氧腺苷自由基(5'-dAdo•)和甲硫氨酸(Met),进而驱动后续的化学转化过程。2010年,康奈尔大学Lin课题组发现了一类非典型的SAM自由基酶——白喉酰胺生物合成酶Dph2,可以引发SAM分子中S−C(γ) 键的均裂, 形成3-氨基-3羧基丙基自由基(ACP•), 进而修饰蛋白质翻译延伸因子EF2的组氨酸残基。
上海药物所黄蔚课题组长期从事多肽/蛋白药物相关研究,致力于发展新颖、实用的修饰新方法(J. Am. Chem. Soc. 2024, 146, 23752; Angew. Chem. Int. Ed. 2024, 63, e202401394; Nat. Commun. 2023, 14, 7169; Angew. Chem. Int. Ed. 2022, 61, e202204132; Angew. Chem. Int. Ed. 2020, 59, 19940),助力多肽蛋白质药物的开发。前期研究表明,在万古霉素中引入硫鎓片段,能显著提高对万古霉素耐药菌株的抑菌效果,同时改善其成药性(Angew. Chem. Int. Ed. 2019, 58, 6678)。延续对于硫鎓的研究兴趣,受上述Dph2酶独特的断键模式启发,研究人员首次开发了一类独特的甲硫氨酸选择性的脱硫编辑策略(图1),显著区别于目前已报道的甲硫氨酸修饰策略(如对甲硫氨酸的硫原子或甲基进行修饰)。该策略先选择性地将甲硫氨酸转化为硫鎓,随后通过光催化模式触发基于硫鎓的分子内自由基取代反应,释放出独特的ACP类自由基,进而被受体所捕获得到稳定的修饰产物;具有反应条件温和,反应效率高,氨基酸兼容性好等优点。
研究人员发现在光催化剂、NHC-BH3还原剂存在的条件下,通过蓝光灯照射,多肽硫鎓可以顺利形成目标自由基,随后与活化烯烃反应形成目标产物。同时对照实验显示,光催化剂、还原剂和光照对反应的发生均至关重要,缺一不可。随后,研究人员成功将不同类型的自由基受体以及功能片段(如糖分子、氟标签、聚乙二醇片段、多肽片段、细胞毒药物等)组装到多肽上,显示出该策略在快速构建多样性多肽偶联物方面的潜力。另一方面,研究人员通过对含有不同氨基酸类型和长度的多肽进行考察,揭示了该策略在氨基酸类型方面良好的兼容性,包括通常在自由基反应中较为敏感的色氨酸、酪氨酸、组氨酸等。同时,该脱硫策略对于含有多个甲硫氨酸的多肽也可顺利实现选择性脱硫编辑,表现出在复杂底物的结构修饰中的潜力(图2)。
近年,相比于常规的线性肽而言,环肽分子以其优秀的代谢稳定性、更好的亲和力和特异性等性质,引起了领域内的广泛关注。在该项工作中,研究人员成功将该策略应用到多肽的环化中,实现了包含N端-侧链相连;侧链-侧链相连等不同连接类型的环肽产物以及单环肽和双环肽等多种环肽产物的构建。该脱硫策略通过碳碳键来构建环肽产物,可以显著增强环肽的代谢稳定性。
最后,自由基捕捉实验显示反应中形成了脱卤芳基自由基和ACP类自由基中间体;对照实验显示碘代芳基对于反应的发生至关重要。同时,DFT计算结果表明在硫鎓分子内自由基取代反应过程中,形成ACP类自由基在动力学和热力学均具有优势,这与实验结果中呈现的断键选择性是一致的。
上海药物所与沈阳药科大学联合培养博士生张玥为论文第一作者,上海药物所刘博博士(现为芝加哥大学博士后)、黄蔚研究员、唐峰研究员为论文通讯作者。本研究得到了国家杰出青年科学基金、国家优秀青年科学基金、国家重点研发计划项目、国家自然科学基金面上项目的基金支持。
原文链接:https://doi.org/10.1021/jacs.5c02226
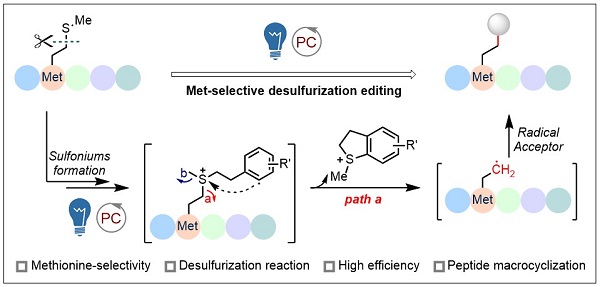
图1. 甲硫氨酸选择性脱硫策略过程
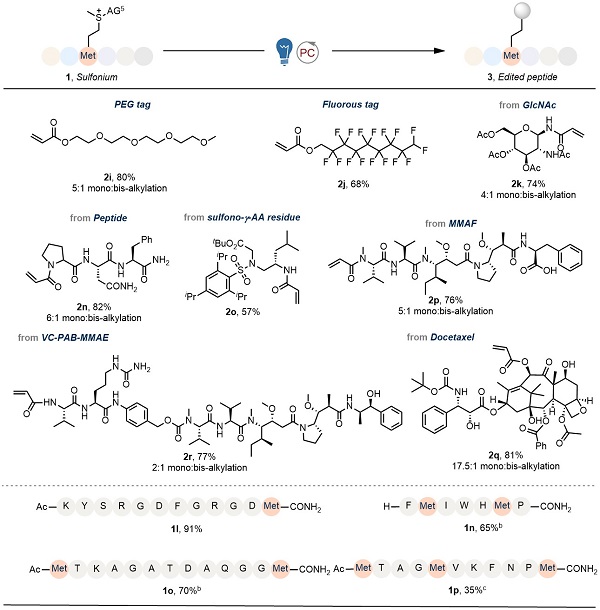
图2. 功能片段的组装及复杂底物的选择性脱硫编辑
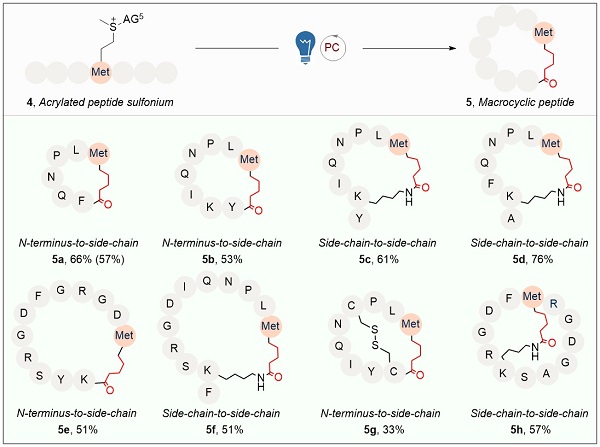
图3. 碳碳键连接的环肽的构建
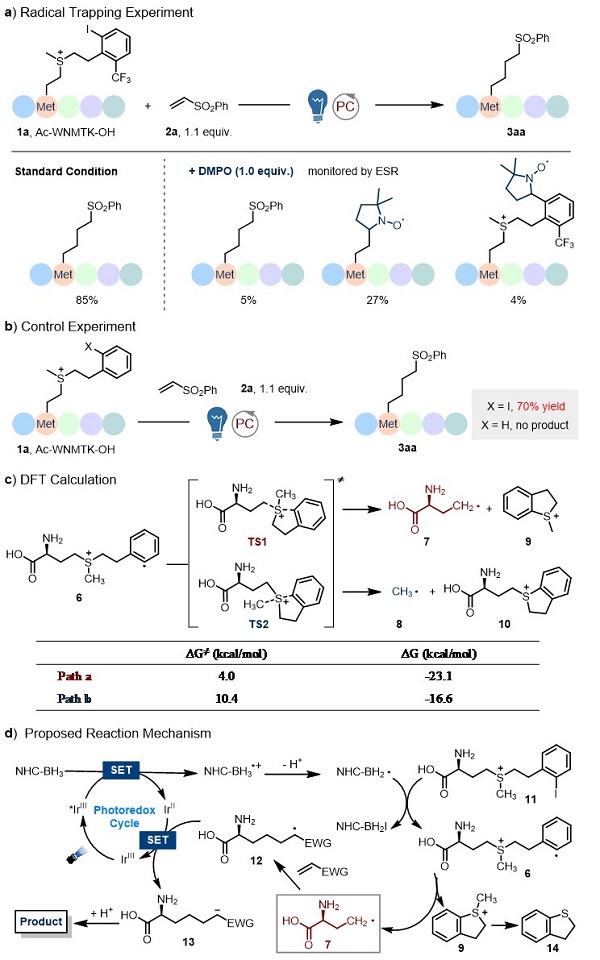
图4. 甲硫氨酸选择性脱硫策略的机制研究
(供稿部门:黄蔚课题组;供稿人:刘博)