上海药物所环状酮亚胺的催化不对称芳基化研究取得进展
手性胺结构广泛存在于众多生物活性天然产物、功能有机分子及手性药物中,因此研究高效的不对称合成方法制备光学活性的手性胺化合物一直是有机化学家们关注的一个重要课题。磺内酰胺(sultam)和磺胺内酯(sulfamidate)是两类含磺酰胺官能团的结构独特的环状胺类化合物,很多具有显著的生理活性,如HIV-1转录酶抑制剂、5-羟色胺拮抗剂、抗肿瘤、抗炎等,此外,它们也是合成很多重要有机和药物分子的关键中间体。手性四取代的磺内酰胺和磺胺内酯通常难以构建,要获得高光学纯度更是挑战。
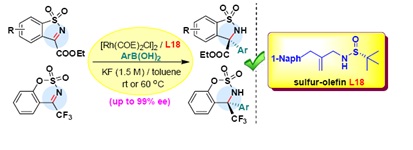
最近,中国科学院上海药物研究所徐明华课题组基于之前提出的新型手性硫烯配体的设计理念(Chem. Commun. 2011, 47, 7230-7232; Org. Lett. 2011, 13, 3410-3413; Org. Biomol. Chem. 2012, 10, 1764-1768),继发现简单直链线性分子骨架手性硫烯配体可以高效催化活化羰基的不对称1,2-加成反应(Angew. Chem. Int. Ed., 2012, 51, 780-783; Org. Biomol. Chem. 2012, 10, 9158-9164; Chem. Eur. J. 2013, 19, 865-869),进一步发展了新的支链结构的手性亚磺酰胺烯烃配体,成功用于铑催化的硼酸对环状酮亚胺的不对称芳基化反应中,首次实现了含季碳手性的相应羧基和三氟甲基取代的系列磺内酰胺和磺胺内酯化合物的高对映选择性合成(最高ee值达99%),为今后这两类结构新颖的手性化合物用于相关药物研究提供了可能。这也是国际上首例手性硫烯配体用于C=N双键的催化不对称加成的报道,研究成果发表在《美国化学会志》(J. Am. Chem. Soc. 2013, 135, 971-974)。自此,结构极其简单的手性硫烯化合物作为配体已在多个催化不对称反应中均表现出独特、优异的立体调控性能,有望在手性药物及中间体合成中发挥越来越重要的作用。
该研究工作得到了国家自然科学基金委员会的支持。
全文链接:http://pubs.acs.org/doi/pdf/10.1021/ja3110818