JACS | 上海药物所构建生物正交诊疗一体化平台同时实现肿瘤成像与靶标蛋白降解
2025年11月28日,中国科学院上海药物研究所张翾课题组与陈奕课题组合作,在国际知名学术期刊Journal of the American Chemical Society在线发表题为“A Versatile Bioorthogonal Theranostic Platform Enables Relay Activation of Tumor Cell Imaging and Targeted Protein Degradation”的最新研究成果。该工作基于生物正交技术构建了新型多功能诊疗一体化平台,可在实现肿瘤细胞成像的同时,通过级联激活机制驱动靶标蛋白的降解,为可控化肿瘤诊疗策略提供了全新的技术路径,对精准肿瘤诊疗具有积极意义。
靶向蛋白降解(TPD)技术是当前药物研发中的前沿策略,可通过分子胶降解剂(MGD)和蛋白水解靶向嵌合体(PROTAC)实现对“不可成药”靶点的精准调控。然而,作为最常用的E3连接酶,CRBN的广泛表达往往会引发健康组织中的非特异性蛋白降解,成为其临床应用的主要限制因素。为突破这一瓶颈,本研究提出了一种适用于CRBN招募型降解剂的通用前药化设计思路,构建了可控释放、具备多重功能的生物正交前药平台,实现了诊断与治疗的有效协同。
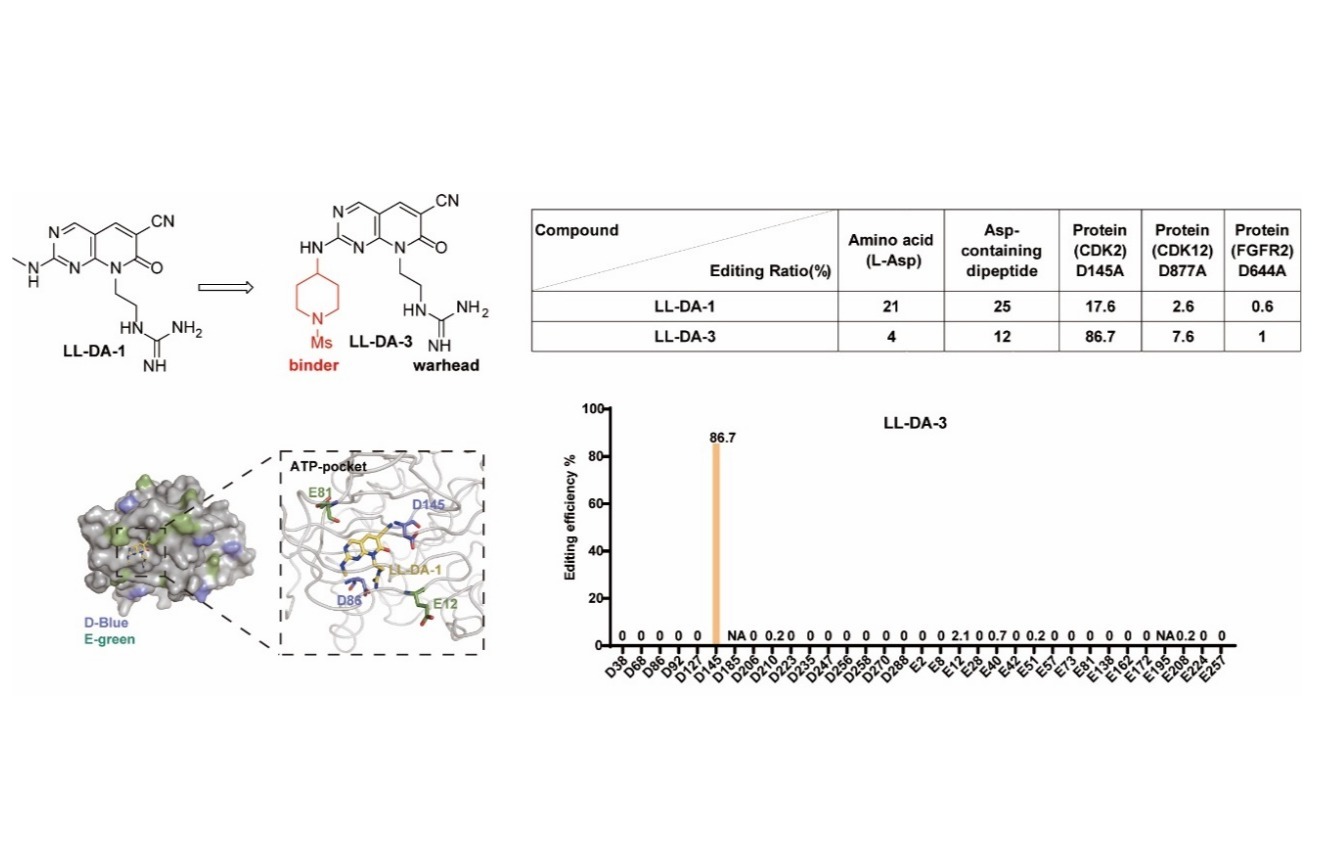
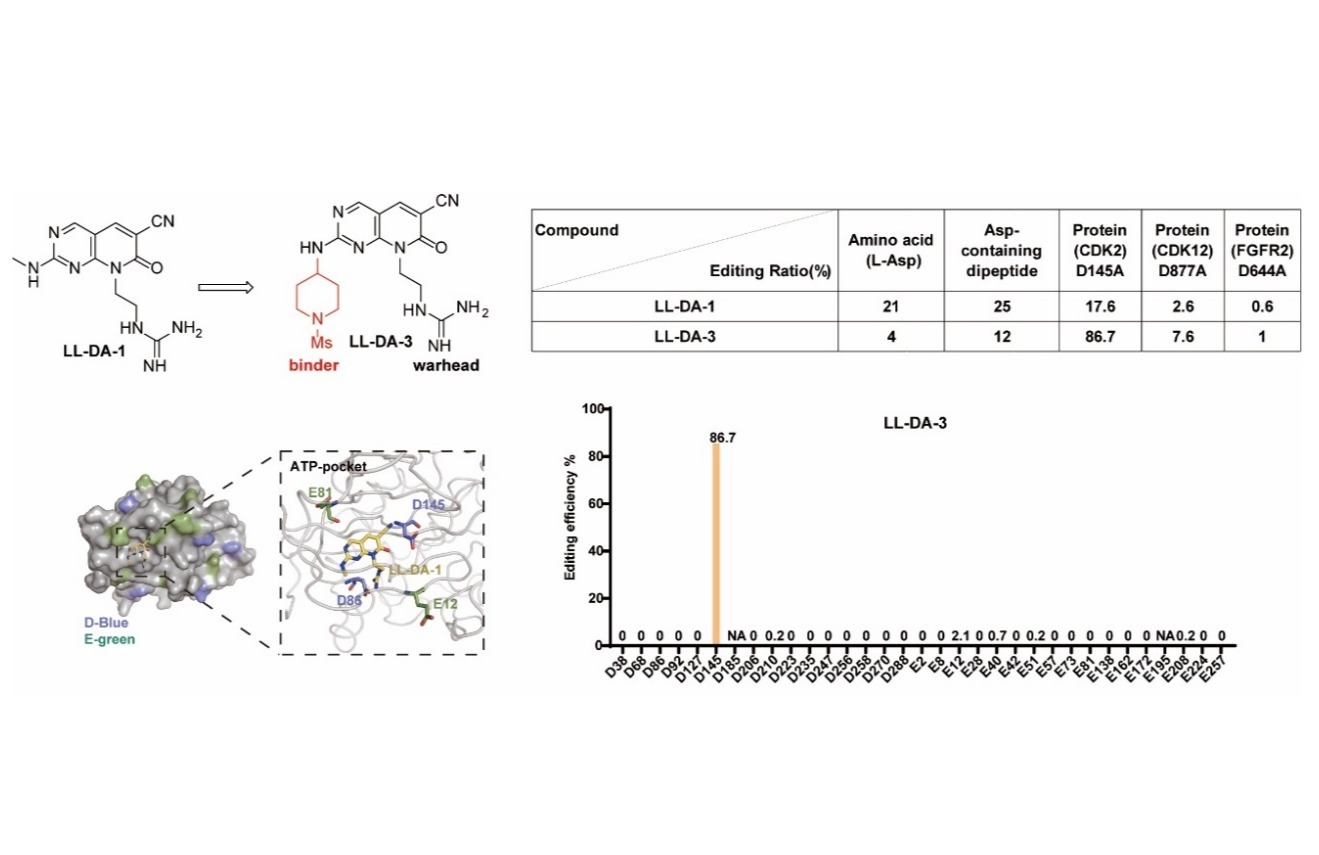
本研究中,研究人员设计了两类功能分子:1)GSH响应型探针分子XZ2223,兼具近红外报告基团与生物正交四嗪触发器功能;2)基于CRBN降解剂的TCO-笼式前药,包括Pro-CC-885和Pro-dBET6。体外实验证明,该生物正交体系可在肿瘤细胞内实现清晰成像,并有效诱导GSPT1与BRD4的降解,而在正常细胞中保持生物学惰性,展现出良好的选择性。值得注意的是,在荷瘤小鼠模型中,联合使用XZ2223与降解剂前药(Pro-CC-885或Pro-dBET6)不仅呈现出优异的肿瘤成像效果,还成功诱导了对应靶蛋白(GSPT1或BRD4)的体内降解。进一步的体内药效研究表明,XZ2223与Pro-dBET6联用的抗肿瘤效果优于母体降解剂dBET6的单药治疗,同时显著降低了全身毒性,充分凸显了该生物正交诊疗一体化平台在拓展治疗窗口方面的独特优势。
上海药物所博士后孙飞龙、上海药物所与南京中医药大学联合培养硕士研究生王恬、上海药物所博士研究生王鹏飞为本论文共同第一作者。上海药物所张翾研究员、陈奕研究员和张秋萌副研究员为本文共同通讯作者。该研究工作还得到了上海药物所朱维良研究员、封晶研究员、陈浩研究员等课题组的大力支持,得到了国家自然科学基金、中国科学院人才计划以及中国科学院战略性先导专项的资助。
全文链接:https://pubs.acs.org/doi/full/10.1021/jacs.5c11564
(供稿部门:张翾课题组)