Adv Sci︱上海药物所在烷基碳苷键的构建方面取得新进展
2024年1月18日,中国科学院上海药物研究所柳红团队与临港实验室王江团队在国际学术期刊Advanced Science上发表题为“Direct Construction of C-Alkyl Glycosides from Non-Activated Olefins via Nickel-Catalyzed C(sp3)-C(sp3) Coupling Reaction”的研究论文。该团队在烷基碳苷类化合物高效合成方面取得突破——使用廉价易得的非活化烯烃作为底物,通过镍催化C(sp3)-C(sp3)偶联实现烷基碳苷的立体选择性构建,为碳苷类化合物提供高效合成方法。
烷基碳苷广泛存在于天然产物以及药物分子中,具有较高的生物活性以及良好的体内代谢稳定性,但目前合成烷基碳苷的方法报道较少,且通常涉及有机金属试剂或Micheal受体等活性试剂。因此如何利用廉价易得的试剂高效构建烷基碳苷类化合物仍然是糖类合成方法学的难点与挑战。
柳红团队与王江团队长期致力于碳苷类化合物高效合成方法学和糖类创新药物研究,并取得了系列成果。目前已经构建了10余种骨架约500个结构多样的碳苷类化合物库,发现新型C,O-螺环芳基碳苷类SGLT2抑制剂LH-1801,目前处于临床III期研究阶段。同时该团队利用碳氢活化方法实现氨基酸烷基碳苷及吲哚-2-脱氧糖碳苷的构建,利用交叉偶联方法高效且立体专一的实现β-脱氧糖碳苷的构建 (Angew. Chem. Int. Ed. 2020, 59, 3491; Angew. Chem. Int. Ed. 2023, 62, e202300424; Adv. Synth. Catal. 2021, 363, 4926)。
本项研究中,该团队采用溴代糖作为糖基底物,利用廉价易得的非活化烯烃作为糖基端位自由基受体,成功发展烷基碳苷类化合物的合成新策略,实现了α构型烷基碳苷类化合物的高效立体选择性合成。
该方法反应条件温和简单,以廉价的NiBr2(diglyme)作为催化剂,二乙氧基甲基硅烷作为氢源,在三齿配体L的作用下,实现溴代糖基底物与非活化烯烃的氢化偶联反应,完成α构型烷基碳苷类化合物的立体选择性构建。该方法无需采用任何导向基或活化基团的辅助,且反应具有广泛的底物适用性,可以耐受环氧环、硼酸酯、羟基等活性官能团。此外,该方法也可以实现天然产物、氨基酸以及肽类分子的后期碳苷化修饰,表现出较强的实用性。同时,研究人员通过自由基捕获实验及氘代实验等对反应机理进行探索。
这一方法为烷基碳苷的构建提供高效合成新策略,为糖类药物的快速发现提供助力。
上海药物所柳红研究员与临港实验室王江研究员为本论文共同通讯作者,上海药物所博士研究生于常跃与硕士研究生徐颖欢为本论文共同第一作者。该项研究获得了国家自然科学基金、国家重点研发计划、临港实验室的资助。
原文链接:https://doi.org/10.1002/advs.202307226
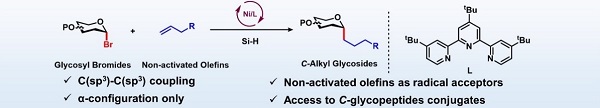
Ni(II)催化烷基碳苷类合成新方法
(供稿部门:柳红课题组)