JACS | 上海药物所在2-乙酰氨基糖直接糖苷化研究中取得新进展
2026年3月11日,上海药物所朱玉根课题组在糖化学高效合成研究方面取得新进展,相关成果以“Partially Protected N-Acetylglycosamine Donors Enable Direct β-O-Glycosylation: Applications and Mechanistic Insights”为题,发表于《美国化学会志》(Journal of the American Chemical Society)。
糖类分子广泛参与细胞识别、免疫调控、炎症应答等重要生命过程,是生命体系中不可缺少的信息分子。其中,N-乙酰氨基葡萄糖(GlcNAc)和N-乙酰氨基半乳糖(GalNAc)是糖蛋白、糖脂、糖胺聚糖以及多种天然活性分子中的重要结构单元。这类糖基通常以特定方式连接到受体分子上,其高效构建对于理解糖链功能、合成活性糖缀合物以及开发糖药物具有重要意义。
这类糖分子的化学合成一直存在难点。原因在于,2-乙酰氨基糖供体在反应过程中往往容易形成一种非常稳定的噁唑啉中间体,使后续成键变得困难。传统解决思路通常需要对乙酰氨基进行多步“保护—脱保护”操作,或者依赖较强酸、高温等较苛刻条件推动反应进行。这不仅会拉长合成路线、降低效率,也常常与复杂分子中的敏感结构不相容,限制了该类糖分子在复杂天然产物、药物分子和功能糖链中的高效引入。
围绕糖分子的高效、精准构建,朱玉根近年来持续开展了系统研究,发展了可规模化制备的8-炔基-1-萘甲酸酯离去基糖供体体系(Chin. J. Chem. 2023, 41, 1305-1312; J. Carbohydr. Chem. 2025, 44, 312-340),实现了羧酸酯类糖苷键的少保护、高效构建(J. Am. Chem. Soc. 2025, 147, 13744-13753)。这些前期工作为本研究中少保护2-乙酰氨基糖供体的设计和反应机理分析奠定了重要基础。
在本项工作中,研究团队针对2-乙酰氨基糖“难以直接糖苷化”的关键瓶颈,设计并发展了一类少保护的2-乙酰氨基糖基8-炔基-1-萘甲酸酯供体(图1)。在金(I)催化条件下,该供体能够与多种醇类和羧酸类受体发生直接、温和且具有高β选择性的O-糖苷化反应。这一策略减少了对繁琐保护基操作的依赖,同时避免了传统强酸条件下强行打开稳定中间体的做法,从而显著提升了合成效率和官能团兼容性。
研究结果表明,该方法适用于多种糖类和非糖类受体,并可用于一系列复杂药物分子的后期糖基化修饰,获得结构明确的2-乙酰氨基糖苷和糖酯产物(图2)。这说明该策略不仅具有方法学意义,也为药物分子的糖基化改造、糖缀合分子的构建以及复杂糖链片段合成提供了实用工具。
在机理研究方面,团队发现,该反应之所以能够在温和条件下顺利进行,与供体分子内部形成的氢键网络密切相关。研究表明,供体中的2-乙酰氨基、3-OH和4-OH之间可以形成协同作用,既有助于削弱分子间聚集,又能促进关键中间体发生一种此前未被认识的开环过程,从而实现高效、选择性的成键(图1)。通俗地说,研究人员巧妙利用了分子内部“自带的相互作用”,让本来很难发生的反应在更温和的条件下顺利完成。该发现为今后发展更多依赖底物自身官能团协同作用的糖化学反应提供了新的思路。
国科大硕士研究生魏靖洋和姜欣洋、澳门科技大学研究生邝板豪为本文共同第一作者。南京中医药大学研究生王晴和李晓龙,遵义医科大学研究生郝邦省和谢飞燕,以及广东药科大学研究生张艺为本文共同作者。上海药物所朱玉根研究员和中山药创院张晓娟博士为共同通讯作者。研究工作得到了中国科学院和中山药创院项目的支持。
全文链接:https://pubs.acs.org/doi/10.1021/jacs.6c00723
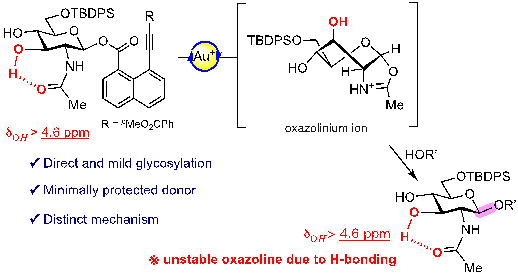
图1. 乙酰氨基糖直接糖苷化反应及其机制
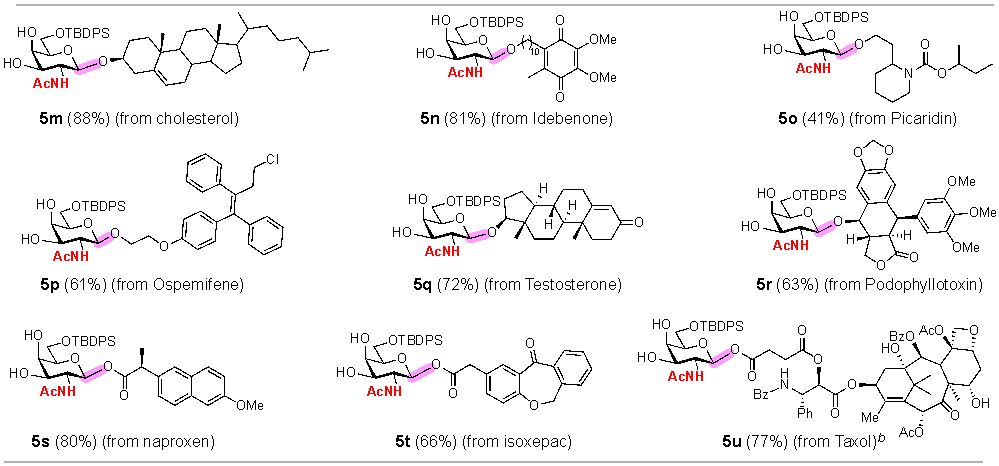
图2. 复杂分子的乙酰氨基半乳糖修饰
(供稿部门:朱玉根)