Cell | 上海药物所合作提出多靶点、多功效药物设计新——“能屈能伸”可变形骨架,“多效多能”新化学分子
北京时间2024年3月28日, 中国科学院上海药物研究所徐华强研究组联合中国科学院分子细胞科学卓越创新中心汪胜研究组,上海科技大学iHuman研究所程建军研究组,于国际学术期刊cell发表题为“Flexible scaffold-based cheminformatics approach for polypharmacological drug design”的研究论文。该研究综合运用化学信息学、结构生物学、在体动物行为学等多学科技术手段,提出了一种名为“基于可变形骨架的化学信息学方法(FSCA)”的全新多靶点、多功效药物设计理念,为治疗复杂精神疾病的药物开发提供了一条新的路径。
精神疾病的治疗一直是医学界的挑战之一。这些疾病的发病机理异常复杂,症状表现也千差万别。传统的单一靶点药物难以满足患者的需求,因此,研发一种能够同时作用于多个靶点的药物变得至关重要。然而,如何设计这种多靶点、多功效药物一直以来都是一个难题。
“北冥有鱼,其名为鲲……化而为鸟,其名为鹏。”庄周在《逍遥游》中描绘了一幅大象无形的绮丽画卷。在不同的情境下,具象可以相互转化。与之类似,多靶点药物分子如同鲲鹏,在结合不同类型受体时也可以发生这样的形态转化,通过调整分子本身构象状态和结合姿势,以适应不同受体口袋的形状,对受体活性进行调节。
以5-羟色胺(血清素,5-HT)1A受体与2A受体为例,这两个受体是许多精神疾病药物的主要靶点。激活5-羟色胺1A受体可改善认知功能,而拮抗5-羟色胺2A受体则可缓解精神错乱症状。因此,研究团队尝试设计同时作用于这两类受体的多靶点、双向活性的化合物分子,以实现双向调控精神疾病症状的目标。该研究融合了化学信息学、结构生物学、细胞功能学实验以及行为药理学等多学科技术手段。通过这些方法,研究团队成功鉴定出通用可变形骨架所应具备的特征,并提出了一种全新的多靶点、多功效活性的药物设计思路。
徐华强团队长期致力于5-羟色胺家族受体的结构与功能研究,并取得了一系列系统性的重要成果。2013年,该团队于在Science上首次报导了激动剂结合的5-HT1B受体的高分辨率晶体结构。2018年,该团队在Cell Discovery发表了首个反向激动剂结合的5-HT1B受体的晶体结构。2021年3月,该团队在Nature上首次报道了5-HT1A、5-HT1D、5-HT1E受体的结构,并揭示了磷脂PI4P(PtdIns4P)和胆固醇调节受体功能的机制和受体的本底激活机制。2021年7月,该团队在Cell Research上首次报道了5-HT1F受体的结构,并揭示了偏头痛药物拉米替坦对该受体的选择性结合机制。2022年5月,该团队在Cell Discovery上首次报道了5-HT5A受体的结构。2022年6月,该团队在Molecular Cell杂志上报道了5-HT4、5-HT6、5-HT7受体与激活型G蛋白(Gs蛋白)和5-HT4受体与抑制型G蛋白(Gi蛋白)结合的复合物三维结构,并提出跨膜螺旋开关调控G蛋白选择性的结构机制。这些在5-羟色胺受体上系统性的研究极大地丰富我们对5-羟色胺系统的结构与功能认识,并为开发治疗抑郁症、精神分裂症、偏头痛等疾病的药物提供了重要基础。
该研究是徐华强团队合作在5-羟色胺系统取得的又一重要成果,这一研究成果深化了我们对于复杂精神疾病药物治疗的药理认知,为未来开发更多、更有效针对复杂疾病的多靶点药物提供了重要的理论指导。
中国科学院分子细胞科学卓越创新中心陈章成博士、余竞助理研究员、上海科技大学iHuman研究所王欢博士、上海药物所徐沛雨博士(现为MIT和Broad研究所博后)为该论文的共同第一作者。分子细胞科学卓越创新中心汪胜研究员、上海科技大学iHuman研究所程建军研究员、上海药物所徐华强研究员为论文通讯作者。此外,北京康迈迪森公司提供了计算资源的重要支持,分子细胞科学卓越创新中心裴钢院士团队在APP/PS1 AD小鼠模型方面提供了协助。该项研究工作得到了国家自然科学基金、科技部重点研发项目、上海市自然科学基金等资助。
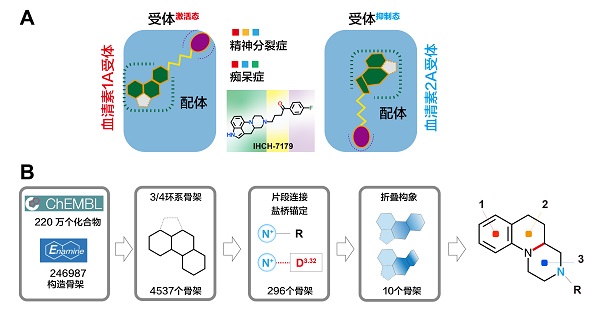
图:(A) 以IHCH-7179为代表的多靶点、多功效活性的药物前体分子的设计理念及其在精神分裂症与痴呆症治疗中的潜在应用;(B)运用化学信息学方法从ChEMBL与Enamine两大化合物库中筛选具备可变构象特征的多环系骨架。