JPBA | 构建通用免疫捕获LC–MS/MS方法,实现人源化IgG1药物精准定量
近日,中国科学院上海药物研究所药物安全评价研究中心研究团队在Journal of Pharmaceutical and Biomedical Analysis上发表了题为“A universal immunocapture LC−MS/MS method for humanized IgG1−based drugs in cynomolgus monkeys”的研究论文。该研究开发了一种通用的免疫捕获液相色谱-串联质谱(LC–MS/MS)方法,可快速并精准地定量人源化IgG1药物,为抗体药物早期非临床研究提供了重要工具。
人源化IgG1抗体药物在癌症、免疫性疾病等治疗领域应用广泛,成为当前生物制药的重要方向。药代动力学(PK)评估是抗体药物开发的核心环节,精准的PK数据不仅有助于理解药物在体内的吸收、分布、代谢和排泄,还为临床剂量设计提供科学依据。随着抗体药物结构日益复杂,开发一种快速、精准且适用范围广的分析方法,成为药物研发中的关键需求。
现有抗体药物PK测定方法多依赖ELISA等配体结合分析(LBA)技术,存在一些局限性。首先,需针对每种药物单独开发特异性的捕获和检测抗体,方法开发周期长,且成本高。其次,血浆或血清中存在的内源性蛋白、抗药抗体(ADA)等干扰物,可影响测定的准确性。最后,LBA方法难以同时覆盖多种药物或抗体衍生物。这些限制导致早期非临床研究效率低,且难以实现多药物并行评价。
为解决上述问题,研究团队开发了一种通用的免疫捕获LC–MS/MS方法。该方法选取人源化IgG1 CH1区域的特征肽GPSVFPLAPSSK作为定量替代物,并结合稳定同位素标记的内标进行定量分析。通过免疫捕获富集抗体,再经胰蛋白酶消化后进行LC–MS/MS 分析,最终通过LC–MS/MS测定特征肽,实现了对人源化IgG1药物的精准、通用定量。该策略不仅消除了对关键试剂的依赖,也可兼顾多药物分析的需求。
团队对血清样品采用了标准化的处理流程。将血清与生物素化抗人IgG1 Fc抗体和磁珠结合,富集目标抗体,并通过多次洗涤去除血清中非特异性蛋白的干扰。富集后的抗体随后经过变性、还原和烷基化处理,提升胰蛋白酶的消化效率,并在消化过程中生成可检测的特征肽,同时加入稳定同位素标记的内标进行定量校正,从而保证测定的准确性和可重复性。最终,样品经LC–MS/MS分析,采用优化的MRM模式和11分钟色谱梯度,实现峰形清晰、信号稳定的定量检测。整个流程经过严格标准化,确保每批样品均可获得可靠且可比的结果。
结果显示,该方法在灵敏度、准确性和稳定性等方面均表现优异。定量检测下限(LLOQ)达0.2μg/mL,且方法验证的各项性能指标均满足ICH M10指南的要求。该方法被应用于两种人源化IgG1药物AB123与MW456的单剂量静脉给药的药代学研究中,IC-LC–MS/MS方法测得的血药浓度与对应ELISA的浓度数据高度可比,且IC-LC–MS/MS方法可同时定量母体抗体及部分降解或修饰形式。
多年来,上海药物所药物安全评价研究中心在数十种抗体类治疗药物(包含人源化单克隆抗体、抗体融合蛋白、抗体偶联药物和多特异性抗体)的药代动力学、免疫原性和毒性评价方面主要采用配体结合技术构建生物分析方法。在完成方法验证后,开展相关样品的分析和数据解读工作。迄今,已在国内外生物分析专业期刊上发表相关文章近20篇,介绍了中心在该领域的特色研究工作。
本研究方法的开发是将配体结合分析技术与液相色谱-串联质谱技术相结合用于大分子抗体药物分析的实例之一。该方法无需依赖特异性关键试剂,适用于所有的人源化IgG1类药物,为多药并行研究提供了可靠的技术支持,尤其适用于抗体药物早期发现阶段的非临床研究,可有效加快人源化IgG1药物的非临床评价的研究进程。
上海药物所联合培养硕士研究生庞佩为本文第一作者,上海药物所宫丽崑研究员、秦秋平正高级工程师与上海应用技术大学林文辉老师为本文共同通讯作者。
原文链接:https://doi.org/10.1016/j.jpba.2026.117461
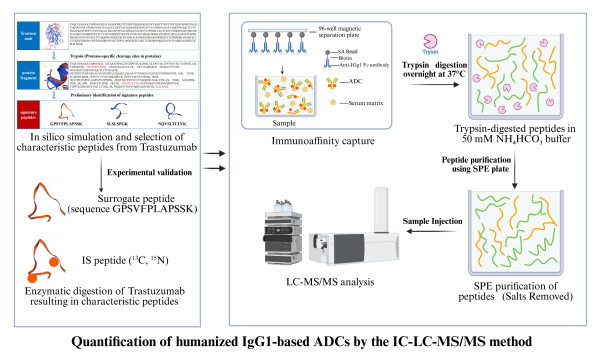
图1. IC-LC–MS/MS方法用于人源化IgG1抗体偶联药物(ADC)的定量分析流程。
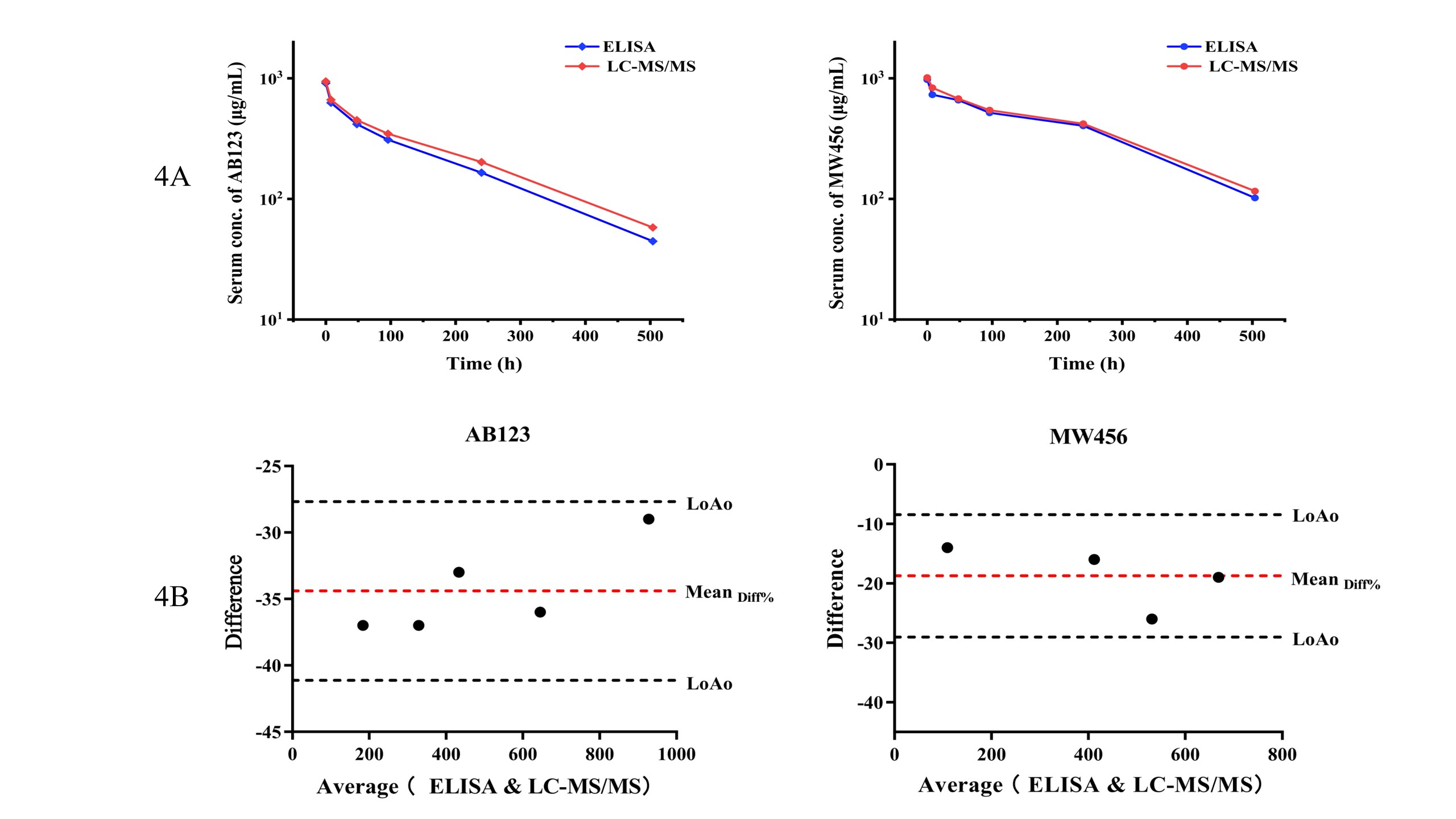
图2. 4A分别展示了AB123(左)和MW456(右)采用LC-MS/MS法(红色)与相关ELISA检测(蓝色)获得的PK曲线。4B通过Bland-Altman分析比较了LC-MS/MS法与 ELISA 测得的AB123(左)和MW456(右)药物浓度。红色虚线表示平均差异,蓝色虚线表示95%一致性界限。
(供稿部门:宫丽崑课题组)