Cell Res | 上海药物所合作揭示靶向HBx-Smc6互作界面抑制HBV的结构与功能机制
2026年4月16日,Cell Research在线发表了中国科学院上海药物研究所王岚峰研究团队、复旦大学袁正宏研究团队与清华大学饶子和研究团队的合作研究成果,论文题为“Structural and Functional Insights into HBx-Smc6 Targeting for HBV Inhibition”。研究揭示靶向HBx-Smc6互作界面抑制乙型肝炎病毒(HBV)的结构与功能机制,为慢性乙肝治疗提供新方向。
HBV慢性感染仍是全球公共卫生领域的重大挑战。HBV慢性感染难以彻底治愈,多数患者经历“肝炎—肝硬化—肝癌”的疾病进程,最终导致死亡。全球每年因HBV相关肝硬化和肝癌死亡近100万人,其中约半数病例来自中国。然而,由于HBV感染在欧美等西方国家发病率较低,全球公共卫生议程及国际顶尖医药研发资源对乙肝的关注相对不足。现有治疗手段(核苷(酸)类似物及与干扰素联用)仅能抑制病毒复制,难以实现彻底清除,患者常需终身服药且存在耐药风险。因此,亟需探索新机制与新靶点。
HBV基因组结构相对“简单”,全长仅约3.2 kb,通过重叠开放阅读框编码表面蛋白、核心蛋白、聚合酶及非结构蛋白(X,HBx)。HBV感染后,其基因组在肝细胞内核修复形成双链闭合环状DNA(cccDNA),作为病毒在细胞核内的长期储存库,是乙肝难以根治的关键因素。HBx在HBV感染的多个关键环节发挥作用,也被认为是关键的致癌蛋白。染色质结构维持蛋白5/6复合物(Smc5/6 complex)被鉴定为宿主限制因子,在HBV感染早期可有效抑制cccDNA的转录活性。为拮抗该宿主防御机制,HBx通过劫持宿主DDB1蛋白,利用CRL4泛素连接酶复合物降解Smc5/6,从而解除对cccDNA转录的抑制。由于HBx蛋白高度无序且结构柔性强,其完整结构及与Smc5/6相互作用的精细机制长期未能阐明,即便借助AlphaFold 3等先进预测工具也难以获得高置信度结构,制约了相关药物研发。
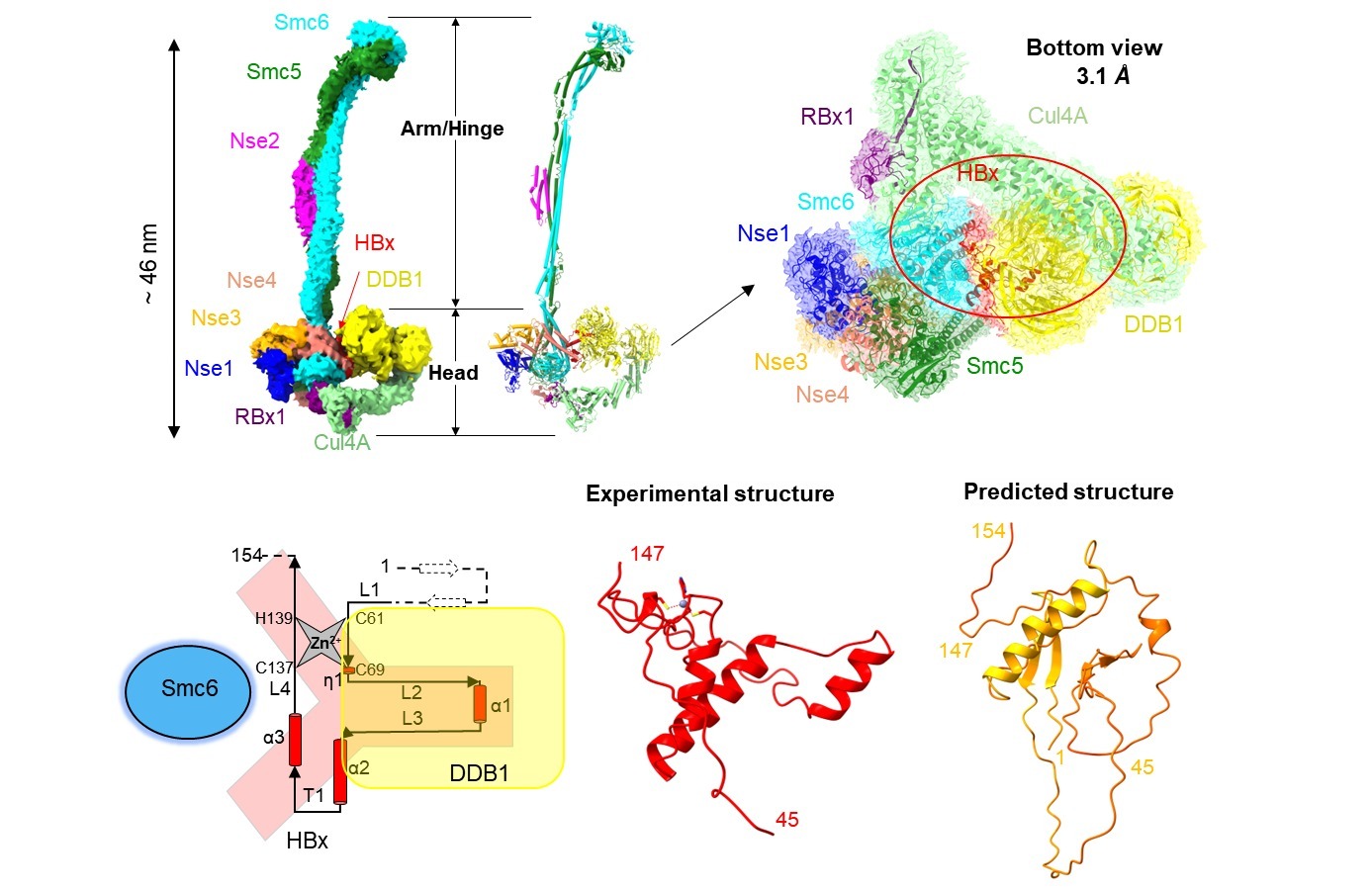
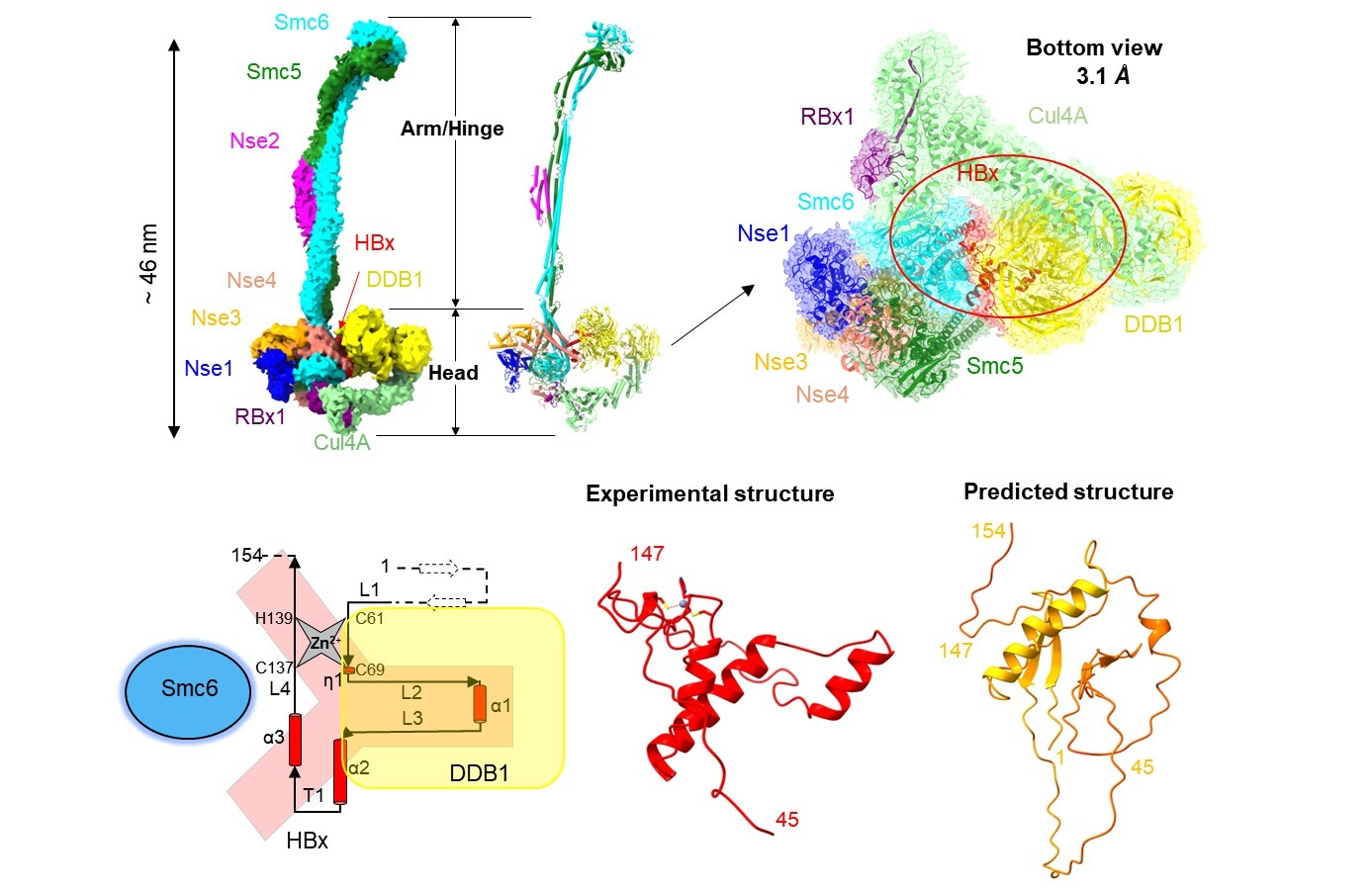
本研究团队利用杆状病毒昆虫细胞表达体系,成功表达并纯化了包含HBx、CRL4及人源Smc5/6复合物的十亚基组装复合物,并采用冷冻电镜单颗粒分析技术解析了其三维结构。研究首次解析了近全长HBx的三维结构,发现其在锌离子稳定下折叠形成独特的Y形构象,与AlphaFold 3的预测结果截然不同。其“下臂”与DDB1蛋白紧密结合,“上臂”则通过由螺旋-转角-螺旋(HTH)基序主导的组合型HTH疏水口袋,精确识别Smc6蛋白表面的“亮氨酸钥匙”(Leucine key)。破坏该互作界面可完全阻断HBx介导的Smc6泛素化降解,并抑制HBV转录与复制。这一精巧的“钥匙-锁”结构,构成了HBx识别并启动Smc5/6降解的分子基础。
Smc5/6复合物在基因组稳定性维持及DNA损伤修复中亦发挥重要作用。哺乳动物感染嗜肝病毒后,其X蛋白介导的Smc5/6降解可导致基因组稳定性受损;此外,慢性感染患者中HBV基因组整合至宿主基因组的比例近乎100%,这些整合的基因可持续表达不同长度的HBx截短突变体,其中带有组成型HTH口袋的突变体可维持对Smc5/6的降解能力。序列比对显示,构成HBx组合型HTH疏水口袋的氨基酸残基在所有HBV基因型乃至数千年前的古代HBV株中均完全一致。嗜肝病毒的进化分析表明,X基因出现于哺乳动物肝炎病毒中,且该疏水口袋高度保守;从宿主角度看,Smc6上的“亮氨酸钥匙”在鸟类中即已出现,并在哺乳动物中完全保守,提示二者存在共进化关系。这与仅在受感染哺乳动物中出现原发性肝细胞癌的表型一致,表明X介导的Smc5/6降解可能对肝细胞癌发生具有重要影响。阻断HBx-Smc6相互作用,有望成为抑制病毒复制并延缓肝炎向肝细胞癌转化的潜在新靶点。
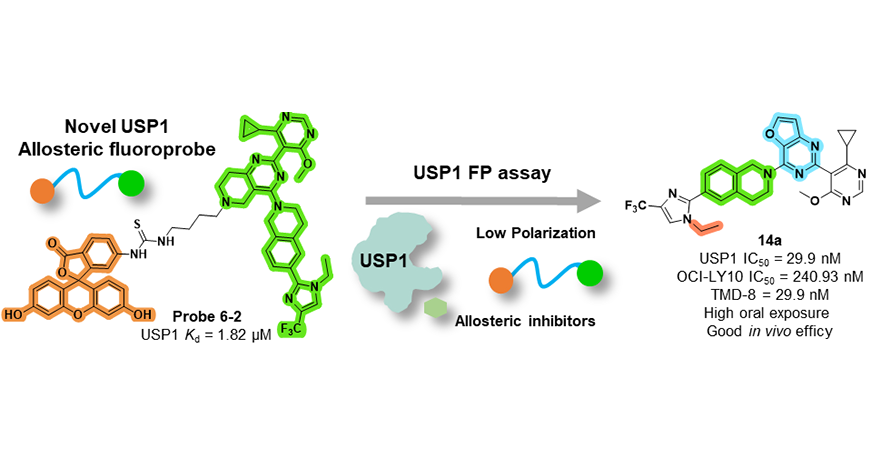
基于这一高度保守且关键的相互作用界面,研究团队对其药物靶点潜力进行了初步评估。通过文献调研及靶向HBx组合型HTH疏水口袋的高通量虚拟筛选,研究者从美国FDA批准的化合物库中成功筛选出小分子化合物Tranilast。该化合物可竞争性结合至HBx的组合型HTH疏水口袋,有效阻断HBx与Smc6的相互作用,从而抑制Smc6的泛素化降解。体外及细胞水平实验均显示其剂量依赖性的抑制效应,为靶向该互作界面的药物研发提供了概念验证。综上,该靶点兼具“双向性”(靶向cccDNA及整合来源HBx)与“双功能性”(抑制病毒复制、防治肝炎-肝癌转化),后续研究将聚焦于此,为乙肝治疗提供新方向。
该工作是继2024年饶子和/胡忠玉/王权研究团队在乙肝表面抗原(HBsAg)如何组装成更高级的纤维以及如何与衣壳相互作用以形成病毒颗粒取得重大突破之后(Wang, Q. et al Science, 2024),科研人员在乙肝基础研究领域的又一重要进展。
上海药物所博士研究生程潼、周金虹,复旦大学博士研究生黄文俊为本文共同第一作者。王岚峰研究员、袁正宏教授和饶子和教授为本文通讯作者。复旦大学陈捷亮教授,上海科技大学高岩和美国加利福尼亚大学圣迭戈分校王红霞亦参与该项研究。该研究获得国家重点研发计划、中国科学院战略性先导科技专项(B类)、上海市市级科技重大专项的资助。冷冻电镜相关工作得到复旦大学和上海药物所冷冻电镜平台的大力支持。
全文链接:https://www.nature.com/articles/s41422-026-01251-7
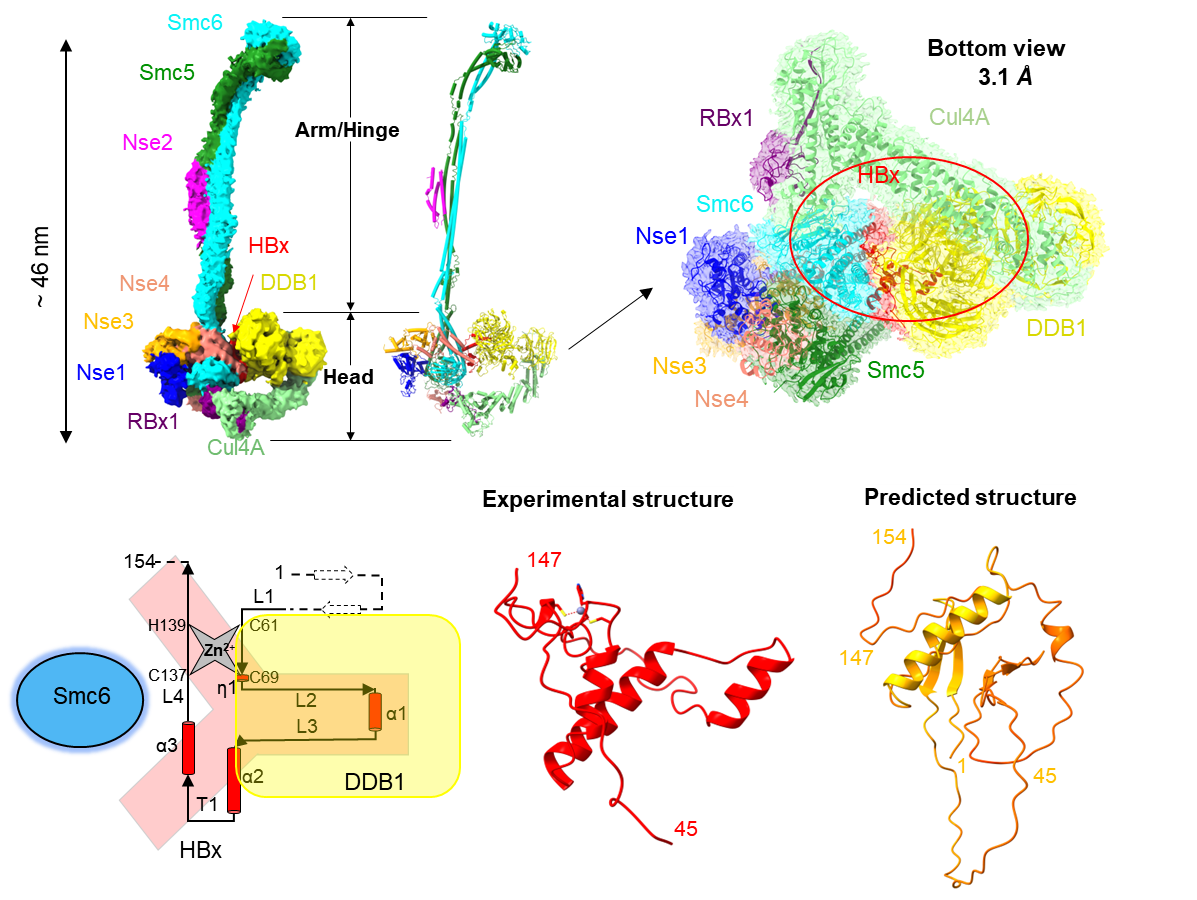
HBx-CRL4-Smc5/6十亚基复合物的结构解析及HBx的高分辨率三维结构
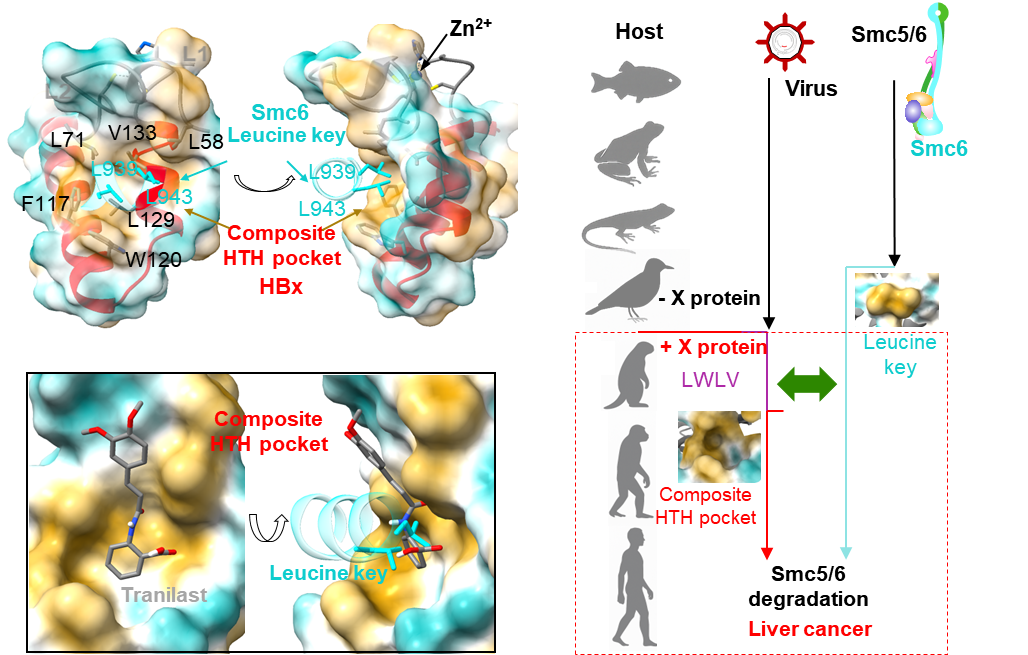
靶向HBx组成型HTH口袋的药物概念性验证
(供稿部门:王岚峰课题组)