JCR | 双载荷设计赋能小分子药物偶联物激活旁观者效应并拓宽治疗窗
2026年2月6日,中国科学院上海药物研究所张翾课题组与中国科学院昆明动物研究所何永捍团队合作,在Journal of Controlled Release期刊发表了题为“Dual-payload small-molecule drug conjugates enable bystander anticancer activity with reduced nonspecific release” 的研究成果,创新性地提出一种双载荷小分子药物偶联物(SMDC,Small Molecule-Drug Conjugate)设计策略。
作为一类极具发展潜力的药物干预形式,SMDC凭借分子量小、组织渗透性强等优势,在肿瘤治疗领域受到广泛关注。然而,传统单载荷SMDC在临床应用中仍存在显著局限,难以兼顾疗效提升与安全性控制。当前,全球SMDC相关研究主要聚焦于靶向配体优化、载荷类型拓展以及肿瘤微环境响应型连接子的开发,但如何在增强肿瘤靶向杀伤效应的同时有效降低毒副作用、拓宽治疗窗口,仍是该领域亟待突破的核心科学问题。本研究创新性地将双载荷策略引入SMDC体系,在实现高效肿瘤靶向递送的基础上成功激活旁观者抗肿瘤效应,并显著降低由药物非特异性内吞引发的毒性风险,从而为SMDC在疗效与安全性之间实现系统性平衡提供了一种全新的设计范式。
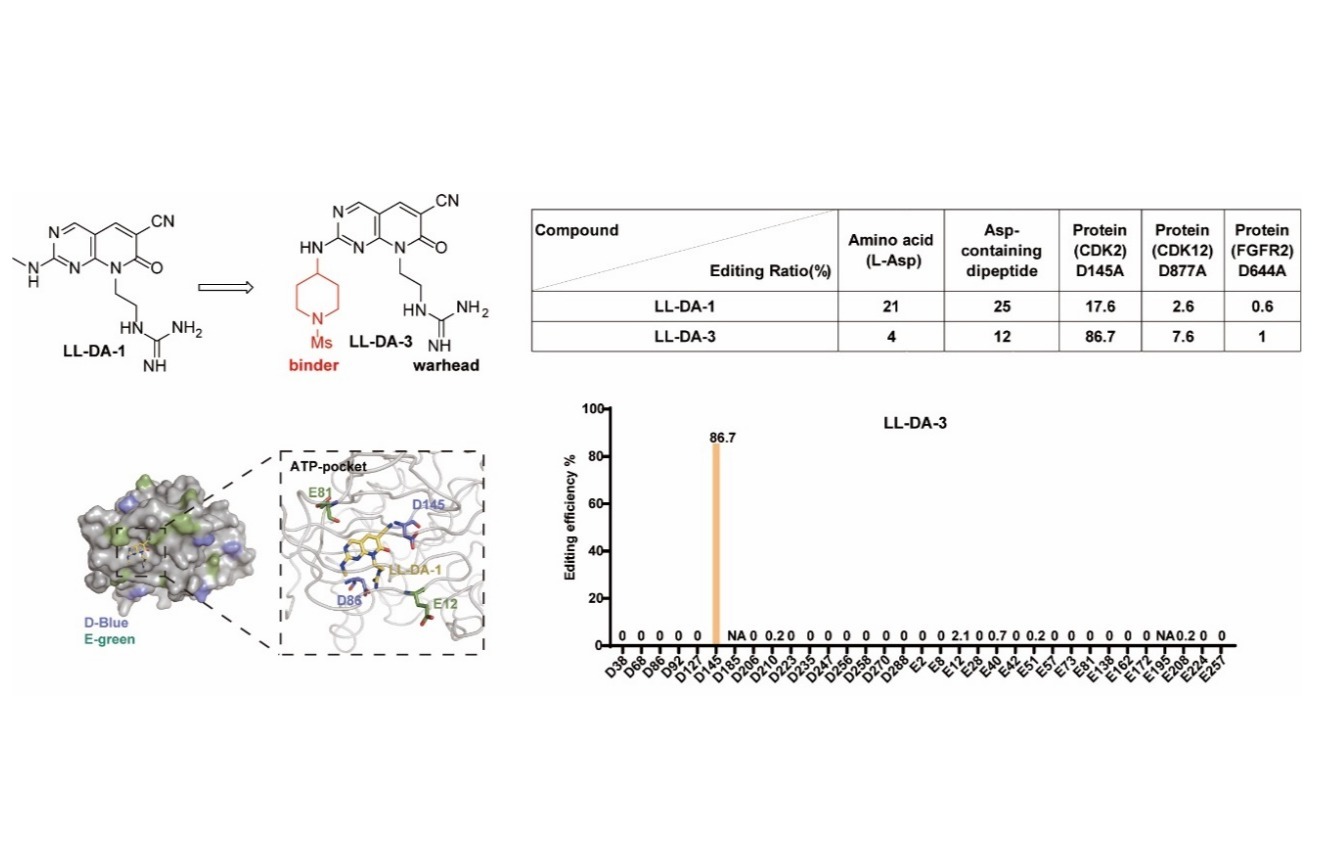
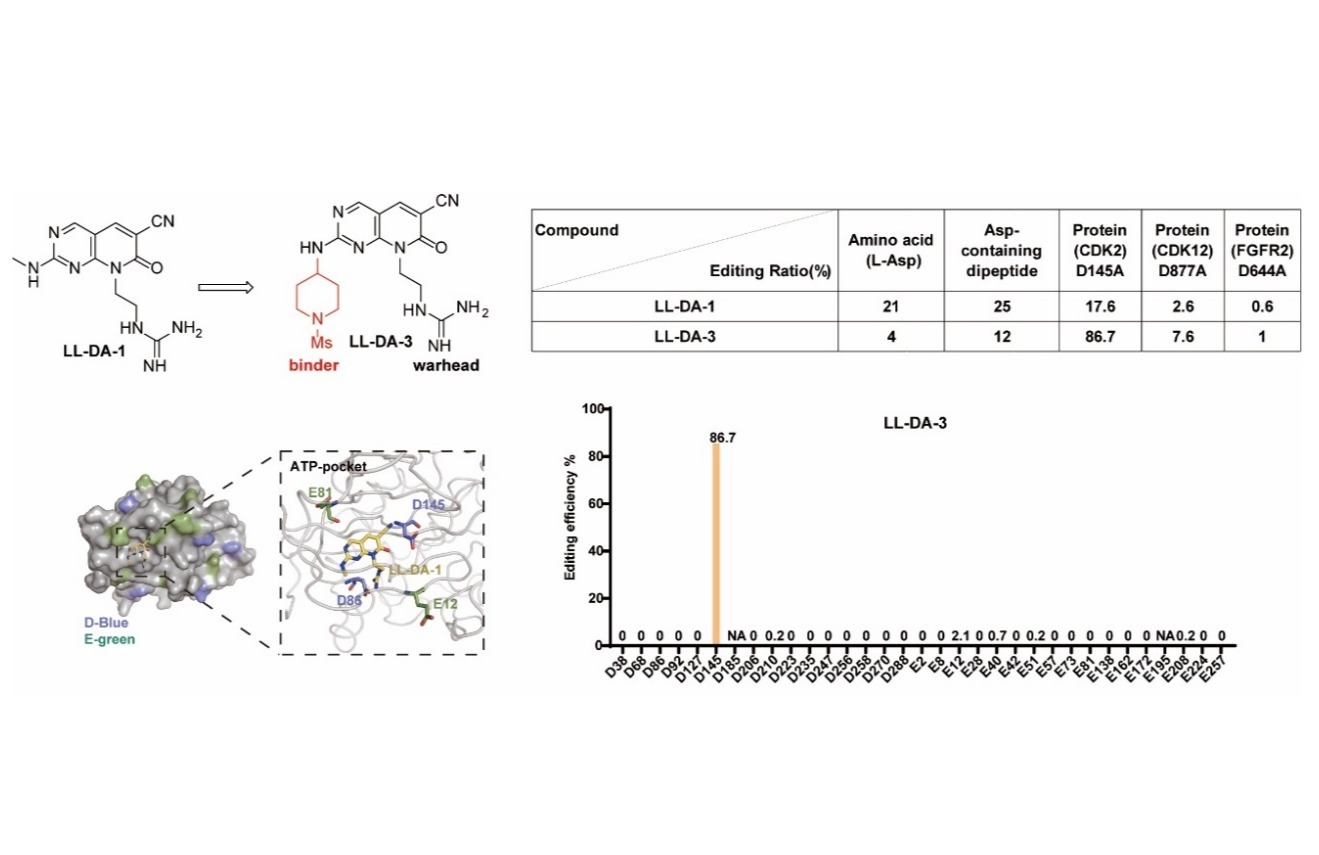
为验证该设计策略的可行性与优越性,研究团队以前期自主开发的肝靶向蛋白降解嵌合体(LIVTAC,Liver-Targeting Chimera)为模型体系,构建了第二代双载荷分子Bi-LIVTAC。体外研究表明,Bi-LIVTAC在ASGPR高表达的肝癌细胞中,展现出优于单载荷LIVTAC的蛋白降解效率和抗肿瘤活性。与此同时,得益于分子尺寸增大及理化性质的优化,Bi-LIVTAC在ASGPR低表达细胞中的被动摄取被显著限制,且其细胞毒性呈现高度受体依赖性,在多种正常细胞系中均未观察到明显毒性,体现出良好的安全性。更为重要的是,研究团队通过体外共培养模型,首次明确证实双载荷SMDC可产生显著的旁观者抗肿瘤效应,对受体低表达的邻近肿瘤细胞具有较强的抗增殖作用,具备克服肿瘤异质性的潜力。在Huh-7肝癌移植瘤模型中,Bi-LIVTAC单药治疗即可产生显著的抑瘤效果,而与一线抗肝癌药物索拉非尼联用,更可实现肿瘤完全消退,且未引发血小板减少等在靶毒性,系统安全性良好。该研究不仅充分验证了双载荷策略在同步提升SMDC疗效与安全性方面的独特优势,而且在不同递送靶点(如叶酸受体)及多类型载荷(如细胞毒素和荧光探针)体系中均获得了成功验证,体现了该策略的广泛适用性与平台化潜力。
上海药物所与中国药科大学联培博士研究生陈川杰、昆明动物所博士研究生潘永涨和沈阳药科大学联培硕士研究生张娜为本论文的共同第一作者,上海药物所张翾研究员和昆明动物所何永捍研究员为论文的共同通讯作者。该工作得到了国家科技重大专项、国家自然科学基金面上项目、中国科学院人才计划等项目的资助。
全文链接:https://doi.org/10.1016/j.jconrel.2026.114695
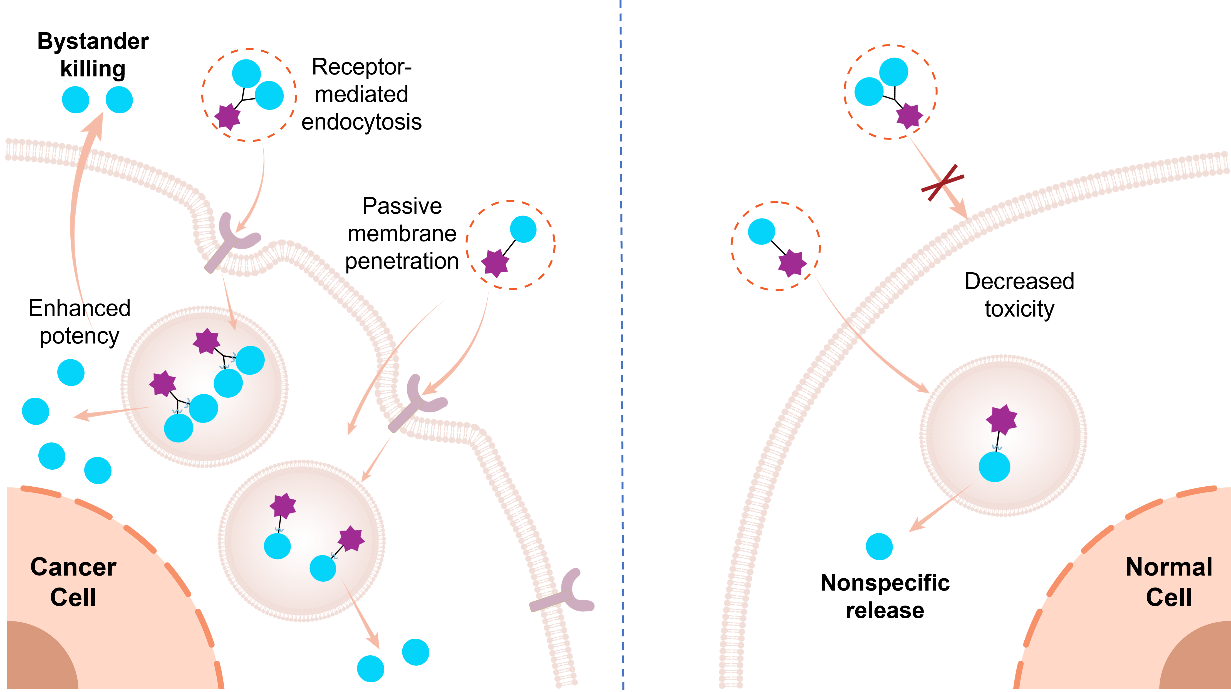
双荷载SMDC设计策略示意图
(供稿部门:张翾课题组)