Angew | 上海药物所合作发现靶向SIRT3的大环磺酰胺类抗帕金森病先导化合物
2024年7月31日,中国科学院上海药物研究所杨伟波课题组合作于Angewandte Chemie International Edition合作发表了题为“Ligand-Enabled Pd-Catalyzed sp3 C‒H Macrocyclization: Synthesis and Evaluation of Macrocyclic Sulfonamide for the Treatment of Parkinson’s Disease”的研究论文。该研究将合成化学和药物化学紧密结合,实现了一类大环磺酰胺化合物的设计与合成,并从中发现了靶向SIRT3的抗帕金森病的先导化合物,为帕金森病治疗提供新思路。
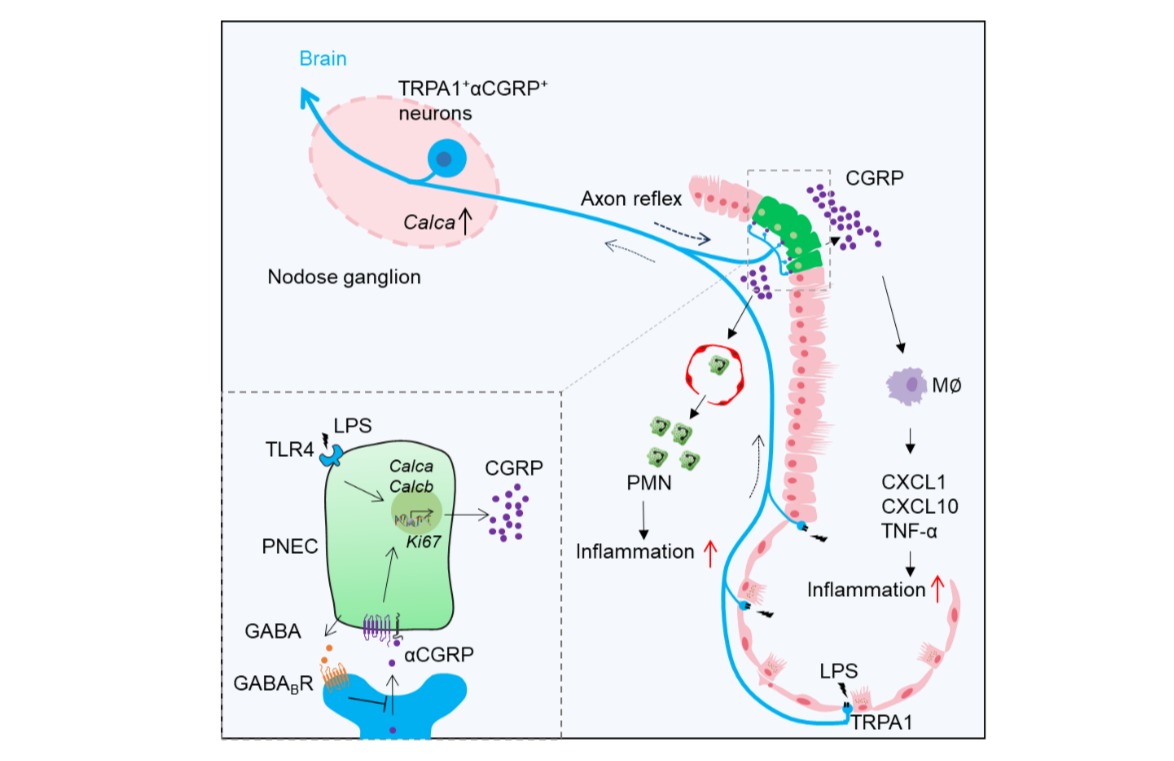
帕金森病(PD)是仅次于阿尔兹海默症(AD)的第二大神经退行性疾病,长期危害中老年人的身体健康,并出现一定的年轻化趋势。其具体发病的机制仍不明确,研究认为主要原因是由于脑部多巴胺能神经元变性、坏死,多巴胺神经递质分泌减少而引起,线粒体功能障碍、神经炎症被发现也与PD密切相关。由于发病机制尚无定论,当前PD的治疗药物非常有限,药物靶点主要局限于中枢多巴胺能系统(如多巴胺前体药物、多巴胺受体激动剂以及多巴胺代谢酶抑制剂等),同时,长期使用这些药物也会带来诸多副作用,科学家们迫切需要寻找新的骨架分子和新的作用靶点,推进抗PD药物研发。
沉默信息调节因子3(SIRT3)是Sirtuins家族的成员,该家族属于NAD+依赖的III类组蛋白去乙酰基酶。SIRT3主要负责调节线粒体功能,而线粒体功能障碍和氧化应激在PD的发病机理中起重要作用。在PD细胞模型中,SIRT3的下调显著降低细胞活力,而SIRT3的过表达可以提高细胞活力,降低细胞凋亡,阻止α-突触核蛋白的积累,同时消除活性氧(ROS),提高模型细胞的生存率。尽管越来越多的研究表明SIRT3的上调在各种PD模型中显示出神经保护作用,然而能用于PD治疗的高活性与低毒性的SIRT3小分子激动剂仍未见报道。
近日,杨伟波课题组与上海交通大学张健教授和浙江大学的徐晓军教授合作,报道了一类靶向SIRT3的大环磺酰胺类抗帕金森先导化合物的发现过程。作者通过仿生模块化策略和新发展的配体介导的钯催化的C(sp3)–H活化大环化方法,设计并合成了一类全新骨架的大环磺酰胺类化合物。虚拟筛选和生物活性测试表明部分大环磺酰胺化合物可以有效激活SIRT3,同时在小鼠帕金森模型中证实了化合物具有治疗帕金森病(PD)的潜力。
在本项研究中,化合物2a可以有效清除PD细胞模型中过表达的α-突触核蛋白。此外,在小鼠行为学上,如转棒、爬杆和旷场实验,2a给药组与对照组相比,可以显著改善模型小鼠的运动功能障碍,其脑组织切片病理学结果进一步显示2a能剂量依赖性提高小鼠黑质多巴胺能神经元数量。重要的是,基因沉默实验结果显示,化合物2a的PD治疗作用与SIRT3密不可分,很可能是通过激活SIRT3来达到其治疗效果的。这一发现为SIRT3作为PD治疗靶点提供了有力佐证,也为PD治疗药物的开发提供了新的分子实体。
上海药物所博士研究生毕童钰、上海交通大学博士研究生崔云霞和中国药科大学博士研究生刘帅为论文的共同第一作者。上海药物所杨伟波研究员、上海交通大学张健教授和浙江大学的徐晓军教授为论文的共同通讯作者。该研究项目得到了国家自然科学基金委和上海市科委等项目的资助。

图1 大环磺酰胺类抗帕金森病先导化合物的发现
全文链接:https://doi.org/10.1002/anie.202412296
(供稿部门:杨伟波课题组)