Nat Methods | SurfDock利用表面信息扩散生成模型实现蛋白质-配体复合物结构的精准预测
近日,中国科学院上海药物研究所郑明月团队开发了一种基于生成式AI的蛋白-配体复合物结构预测方法SurfDock。该方法通过利用蛋白质表面信息构建几何扩散神经网络,高精度自动生成配体结合构象,并已成功应用于基于结构的虚拟筛选。相关研究论文"SurfDock is a surface-informed diffusion generative model for reliable and accurate protein–ligand complex prediction"于2024年11月27日在Nature Methods在线发表。

理解蛋白-配体相互作用是分子生物学和生物化学的基础。从酶催化到信号传导,这些相互作用构成了众多细胞过程的核心。对蛋白-配体相互作用的深入理解对基于结构的药物设计至关重要,研究人员可以据此发现或设计与特定蛋白质结合的配体。基于人工智能(AI)技术,我们能更精准地理解蛋白-配体相互作用,加速药物发现的进程。人工智能与生命科学的交叉正在改变人类健康和医学研究的格局,为疾病研究和靶向治疗药物开发开辟新的途径。
在这项工作中,研究团队提出了一种新型基于蛋白表面的几何扩散网络SurfDock,用于生成精准可靠的蛋白-配体复合物构象(图1)。该模型将多种蛋白质信息(包括表面特征、残基结构特征和预训练序列特征)整合到表面节点的表示中,并配备了一个称为SurfScore的内部评分模块,通过对蛋白-配体复合物的训练来评估构象的置信度。图2展示了SurfDock对接的动态过程。此外,SurfDock还整合了一个可选的基于力场的优化步骤,进一步提升了其性能。这些创新设计使得SurfDock在多个基准测试中展现出优异的对接能力,其生成构象的合理性显著超越了现有的深度学习方法。值得注意的是,SurfDock能够有效地适应新的蛋白质、口袋和空(apo)结构,即使在处理高度柔性的配体时也表现出色。在实际应用中,研究团队通过针对ALDH1B1的筛选实验证实了SurfDock的实用价值,成功的快速筛选出七个具有新骨架的先导分子。
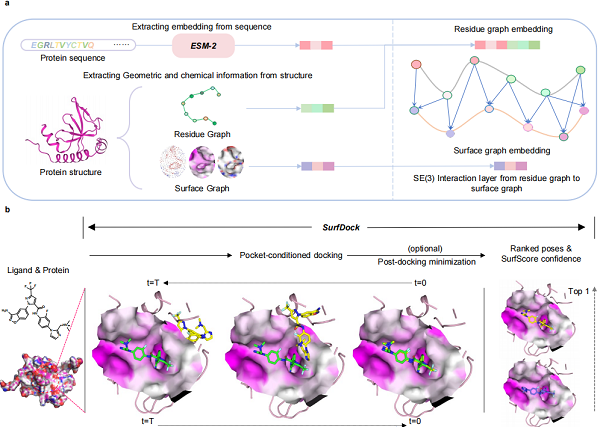
图1. SurfDock 架构图。a: SurfDock中蛋白质多模态表征示意图。b: SurfDock工作流程概述。
浙江大学与上海药物研究所联合培养博士研究生曹端华,上海科技大学与临港实验室联合培养博士研究生陈铭安和上海药物所硕士研究生张润泽为本文的共同第一作者。上海药物所郑明月研究员为本文通讯作者。本研究得到了国家自然科学基金、国家重点研发计划、上海药物所与上海中医药大学中医药创新团队联合研究项目、中国科学院青年创新促进会会员项目、上海市科技重大专项等项目的资助。
图2. SurfDock对接的动态过程可视化示例。
原文链接:https://www.nature.com/articles/s41592-024-02516-y