Small Struct |上海药物所合作构建递送纳米粒的纳米网格新载体
脂质体、外泌体等纳米制剂在疾病治疗领域已有广泛应用,但仍存在体内停留时间短、清除速率快等挑战,合适的递送载体可改善其体内行为,达到更好的治疗效果。关于药物分子的递送研究已持续几十年,而对于纳米粒递送的研究却极少,且分子水平的治疗剂适用的载体通常无法递送纳米粒。所以,制备生物安全、具有开放孔道、孔径在纳米尺度范围的多孔载体,用于纳米粒的递送,将为药物递送开辟新思路。
2024年1月30日,中国科学院上海药物研究所张继稳团队与沈阳药科大学王淑君团队联合在Small Structures上发表了题为“Supramolecular Nano-Grid Platform to Load and Deliver Liposomes and Exosomes”的研究论文。该研究以环糊精为基本结构单元,构建了一种新型的纳米网格结构载体,其不仅具有pH/H2O2双响应性,还能通过多孔网状的纳米结构负载脂质体和外泌体:将脂质体靶向递送到肺部并延长其体内作用时间,实现外泌体递送并达到长时间释放效果。
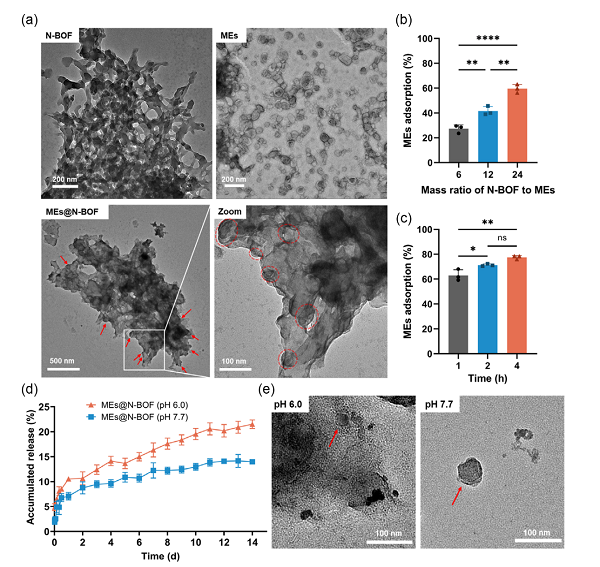
研究人员基于环糊精金属有机骨架的有序结构,针对环糊精单元上不同位点的羟基活性差异,采用对称型硼酸酯键交联剂,对其进行交联,通过控制反应条件,得到纳米网格状和球形两种不同结构特征的硼化有机骨架(BOF)。其中,纳米网格状结构由数十纳米直径的纤维交织而成,分布有10-300 nm的开放空间。硼酸酯键交联剂赋予BOF以pH/H2O2双响应性,其在生理pH环境下稳定、在炎症或肿瘤内环境下迅速降解,在pH 7.4时的半衰期是pH 5.0的467倍,H2O2存在时降解速率显著加快。
纳米网格结构和球状结构的BOF
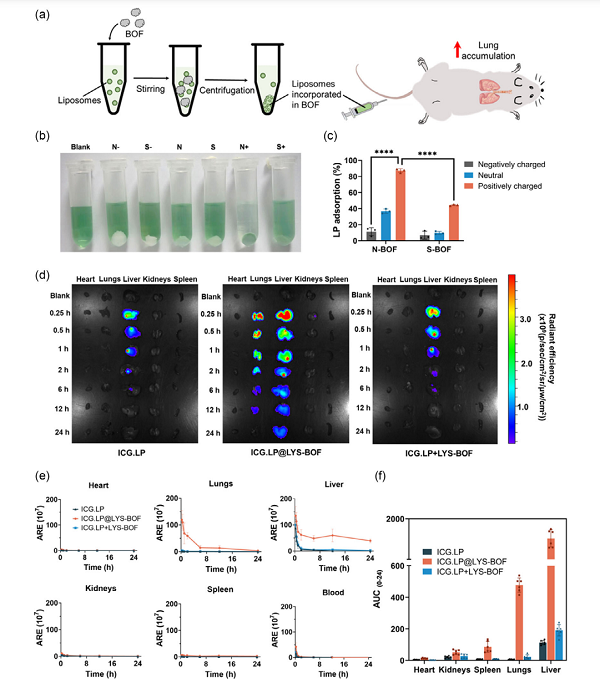
研究表明,纳米网格状结构的BOF(N-BOF)比球状BOF(S-BOF)具有更好的脂质体俘获效果,并能显著改变脂质体在小鼠体内的生物分布:游离脂质体在肺部几乎没有分布,负载于N-BOF后,脂质体在肺部的荧光信号显著增强,肺部生物利用度提高约90倍。
N-BOF的脂质体负载能力及对脂质体生物分布的影响
牛奶外泌体的粒径为50-150 nm,处于N-BOF孔径的主要分布范围内。N-BOF对牛奶外泌体具有良好的俘获效果,利用透射电镜可以观察到脂质双层结构的外泌体分布在N-BOF颗粒上。N-BOF能够响应性释放所负载的外泌体,在pH 7.7环境中,14天内N-BOF对外泌体的释放量为14%,而pH 6.0环境下释放量则为21%,且释放出的外泌体仍能保持完整的结构。
N-BOF对牛奶外泌体的俘获及pH响应性释放
上海药物所硕士研究生李晶为本文第一作者,上海药物所硕士研究生马武珍进行了外泌体部分的研究,沈阳药科大学博士研究生杨伯阳完成脂质体制备。上海药物所张继稳研究员、伍丽副研究员和沈阳药科大学王淑君教授为本文共同通讯作者。该研究得到了国家自然科学基金和国家重点研发计划等项目的资助。
(供稿部门:张继稳课题组;供稿人:李晶)