2024年2月10日,中国科学院上海药物研究所徐华强/吴灿荣团队与华中科技大学同济医学院附属同济医院在Science Advances合作发表了题为“Molecular Recognition and Activation of the Prostacyclin Receptor by Anti-Pulmonary Arterial Hypertension Drugs”的研究成果。本研究利用冷冻电镜技术解析了曲前列环素(TRE)和赛乐西帕在体内的活性代谢物MRE-269(MRE)两种药物结合于人类前列环素受体-Gs复合物的结构,分辨率分别为2.56埃和2.41埃(图1)。这项研究揭示了IP独特的配体选择性、受体激活以及G蛋白偶联机制,有望为更高选择性的IP激动剂提供结构依据。
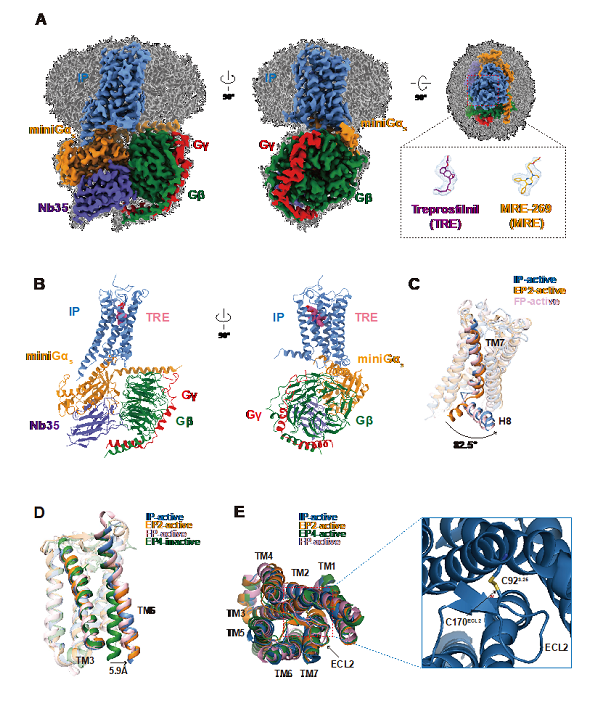
图1. IP-Gs与配体复合物的冷冻电镜结构。
前列腺素是一类含氧花生四烯酸代谢物,包含前列环素(PGI2)、前列腺素 F2 (PGF2 )、前列腺素D2 (PGD2)、前列腺素 E2 (PGE2)、血栓素A2 (TXA2)。它们通过作用于对应的前列腺素受体发挥广泛的生物学功能。其中前列腺环素受体(IP)在配体作用下激活后主要与Gs亚型的G蛋白偶联,激活腺苷酸环化酶并催化三磷酸腺苷(ATP)转化为环磷酸腺苷(cAMP)。IP在肺脏和心脏中大量分布,在血管内皮细胞和平滑肌细胞中表达量较高,激活时具有促进血管舒张、抗血小板、抑制增殖以及免疫调节的作用,在调节血压和炎症反应中发挥了重要功能。因此,它是治疗肺动脉高压的重要药物靶点,其选择性激动剂在PAH高压的治疗中起到了重要作用。
在临床上,目前已经有包括依前列醇(Epoprostenol),曲前列环素(Treprostinil,TRE)和赛乐西帕(Selexipag)在内的数种选择性IP受体激动剂被美国食品和药物管理局 (FDA)批准用于治疗肺动脉高压。其中依前列醇是IP的内源性配体,由于稳定性较差,只能用于静脉给药。曲前列环素作为内源性配体类似物,稳定性有了较大提升,可以口服给药,但因其选择性较差,所以存在较多的副作用。赛乐西帕是FDA于2015年批准的用于治疗肺动脉高压的IP选择性激动剂,相较于其他IP激动剂,赛乐西帕具有更高的选择性和更长的半衰期。在体内代谢为MRE-269后,能够以较高的选择性激活IP,达到治疗肺动脉高压的目的。作为肺动脉高压的重要治疗靶点之一,开发具有更高选择性和稳定性的IP激动剂,是改善肺动脉高压病人预后、降低毒副作用和提高生活质量的关键。然而,目前IP与其选择性配体复合物的关键结构缺失,有关IP的配体识别、激活机制和决定药物选择性的分子机制等科学问题目前尚未解决,这也极大阻碍了IP高选择性激动剂的开发。
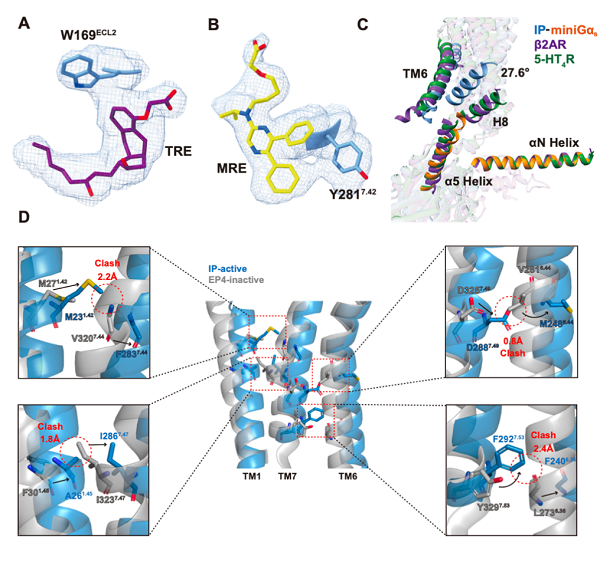
在本项研究中,通过结构解析、功能实验和分子对接,科研人员揭示了脂质受体家族中IP的配体选择性识别、激活以及G蛋白偶联方面的独特机制。通过对比两个药物与IP的相互作用氨基酸的差异,研究人员发现,曲前列环素(TRE)在与保守的W169有着较强的π-π 相互作用,与不保守的氨基酸Y281则结合很弱,而MRE-269则刚好相反,在避免了与保守氨基酸W169结合的同时,与不保守的氨基酸Y281有着较强的π-π相互作用。这种相互作用氨基酸的差异可能是MRE-269选择性明显高于曲前列环素(TRE)的分子机制(图2)。在激活机制方面,IP并没有典型的W6.48 ‘toggle switch’,且两个配体分子距离TM6都距离较远。作者通过与同家族抑制态结构对比和功能实验发现,IP在配体作用下引起TM1的内移,进而通过TM1-TM7-TM6逐步传递,引起受体的激活(图2)。
图2. IP受体的激动剂选择性、激活和G蛋白偶联机制。
本研究的冷冻电镜数据在上海市高峰电镜中心收集。上海药物所与华中科技大学同济医学院附属同济医院联合培养硕士研究生汪骥齐是该论文的第一作者。上海药物所为本研究第一完成单位,上海药物所吴灿荣副研究员、徐华强研究员为该论文的共同通讯作者。该工作获得了包括国家自然科学基金委、科技部和中科院先导专项以及上海市市级科技重大专项等项目的资助。
(供稿人:汪骥齐)