J Control Release | 上海药物所合作开发新型单链DNA载体的基因治疗系统
2026年2月27日,中国科学院上海药物研究所郝沛研究组与临港实验室李洪林、华东理工大学刘雪婷、中国科学院分子植物科学卓越创新中心李轩等研究组合作,在国际知名学术期刊Journal of Controlled Release 在线发表了题为 “Lipid nanoparticle (LNP)-mediated cytoplasmic expression of single-stranded DNA and its application in Mpox vaccine”的研究论文。该研究开发了一种新型单链DNA(ssDNA)和纳米脂质体(LNP)结合的基因治疗递送系统。该系统利用单链DNA模板纳米脂质体(LNP)的适配性,实现了ssDNA-LNP体系的高效递送和长期表达稳定性,同时,还利用T7RNA聚合酶(T7RNAP)实现了完全独立于细胞核、细胞质内高效转录与翻译,为核酸疫苗及治疗药物的开发提供了一个全新的技术路径。
目前,以LNP为核心的mRNA递送体系在核酸疫苗开发中展现了里程碑式的意义,但其固有的不稳定性导致细胞质半衰期较短,蛋白表达通常在24小时内迅速下降,难以满足需长效表达的临床场景。虽然自扩增RNA(saRNA)可延长表达时长,但其巨大的分子尺寸(约9.3 kb)不仅增加了LNP封装难度,其病毒来源的复制酶还易引发强烈的免疫反应。相比之下,DNA系统虽具备优异的稳定性,但常规双链DNA(dsDNA)高度依赖效率极低的入核过程,且其50nm的持久长度赋予的高刚性与LNP封装环境并不兼容,更易激活cGAS-STING通路导致严重的炎症副作用。
针对这些瓶颈,研究团队开发了LNP-ssDNA-T7RNAP模块化基因递送系统。该系统的设计灵感源于对DNA稳定性与mRNA胞质作用优势的深度整合:利用LNP共同递送单链DNA(ssDNA)模板与T7 RNA聚合酶(T7RNAP)。ssDNA在物理特性上兼具分子柔韧性与较小的流体力学体积,使其能像mRNA一样被高效包裹进LNP中。进入细胞后,T7RNAP在胞质内直接驱动ssDNA模板的高效转录,通过IRES元件介导翻译,完全绕过了细胞核这一天然效率屏障。由于不涉及病毒复制酶及双链RNA中间体,该系统表现出极低的免疫原性。
为了将这一概念验证推向应用,研究人员对系统进行了多维度的系统优化,包括补体引物长度筛选、共递送比例测试及ssDNA模板的化学修饰等优化策略。这些方法确立和完善了LNP-ssDNA-T7RNAP系统的胞质高效表达,使其成为一个低免疫原性、高性能的基因表达工具。为评估该系统在临床治疗的应用潜力,研究团队设计并构建了编码猴痘病毒L1R和A33R两种表面抗原的ssDNA疫苗,对小鼠进行单剂量接种并持续监测28天内的免疫应答动态。实验结果显示,该系统展现出优异的免疫持久性和稳健的体液免疫应答。接种后仅7天,小鼠体内即可检测到明显的抗原特异性IgG抗体。值得注意的是,在与常规mRNA疫苗的对比实验中,mRNA组在接种21天后抗体水平已表现出下降趋势,而LNP-ssDNA-T7RNAP疫苗组的抗体滴度在整个28天的观察期内依然保持持续攀升趋势。这种显著的表达动力学差异证明了基于ssDNA模板的胞质转录体系能够克服常规mRNA疫苗短效表达的局限,提供更长效的抗原刺激。进一步的安全性评价实验显示,虽然疫苗诱导了必要的先天免疫激活(如IFN-γ和CXCL10的上升),但促炎因子水平远低于系统性炎症毒性的阈值,且未见明显的肝肾毒性。这一系列数据充分证明,LNP-ssDNA-T7RNAP递送系统在实现高效、长效基因表达的同时,兼具良好的生物安全性和耐受性。
综上,LNP-ssDNA-T7RNAP系统成功桥接了DNA稳定性与mRNA胞质作用优势,通过模块化设计实现了高效的非病毒基因递送。该研究不仅规避了传统DNA递送的入核难题和基因组整合风险,还显著改善了核酸药物的表达时长。
上海药物所郝沛研究员为该论文的通讯作者,分子植物卓越中心李轩研究员、华东理工大学刘雪婷教授及上海临港实验室李洪林教授为该论文的共同通讯作者。华东理工大学与分子植物卓越中心联合培养博士研究生张凯翔及临港实验室博士后刘彩霞为论文共同第一作者。该项工作得到了中国科学院战略先导科技专项和国家自然科学基金等项目的支持。
原文链接:https://doi.org/10.1016/j.jconrel.2026.114740
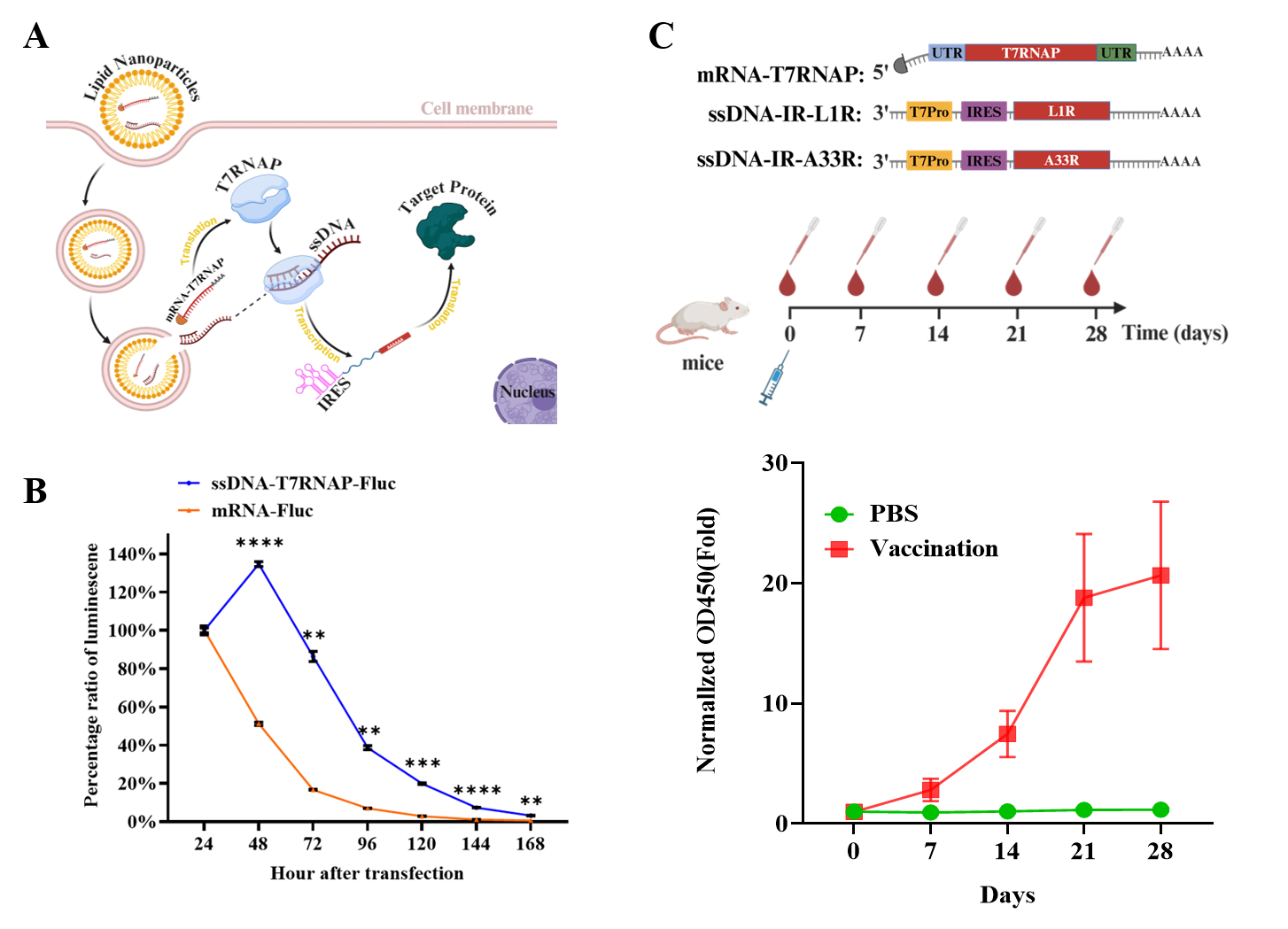
图:LNP-ssDNA-T7RNAP系统工作原理及猴痘疫苗免疫评价。(A)LNP-ssDNA-T7RNAP系统工作原理示意图。(B)LNP-ssDNA-T7RNAP系统与mRNA系统的表达动力学比较。(C)猴痘疫苗小鼠免疫实验。
(供稿部门:郝沛课题组)