ACS Nano封面 | 上海药物所合作开展气管靶向递药系统设计与跨尺度三维表征
2025年6月5日,中国科学院上海药物研究所张继稳团队联合临港实验室殷宪振团队,在ACS Nano上合作发表了题为“Tracheal targeted nanogrid delivery systems of dexamethasone visualized by single-particle tracing and multiscale pathological mapping”的研究论文,并被选为封面文章。


肺部病理微环境具有高度的时空异质性,相关药物递送面临多重挑战。传统二维(2D)研究手段难以跨尺度表征纳米制剂在肺部的生物分布,极大限制了递药系统的靶向性评价。为突破这一瓶颈,合作团队开展了面向生命体的结构药剂学研究,致力于在三维(3D)空间和单细胞水平上构建全肺病理图谱。一方面,依托3D病理图谱评价纳米制剂的靶向治疗效果;另一方面,关注纳米粒在全肺内的跨尺度分布规律。该研究基于交联环糊精纳米网格材料(GCC),结合单颗粒示踪与3D病理图谱,在单细胞分辨率上实现对纳米粒在气管外周的精准定位,开展3D药效学评价,完成从制剂结构到生理结构的跨尺度关联分析,为肺部疾病的精准治疗提供结构药剂学新策略。
与传统立方体形状的环糊精交联物颗粒相比,具有独特网格结构的GCC-Rh110在经小鼠尾静脉注射后,表现出显著的气管外壁聚集特征。GCC负载地塞米松(DEX)后,有效延长了药物的体内滞留时间,药代动力学结果证明DEX@GCC具有明显的缓释特性。此外,GCC具有广谱抗氧化的优势,可以高效清除超氧根阴离子和羟基自由基等多种活性氧,结合其气管靶向优势,为气管相关肺部疾病的精准治疗提供了新的思路。同时,该研究建立的全肺3D可视化方法为纳米制剂的跨尺度研究提供了重要技术支撑,具有广泛的应用前景(图1)。
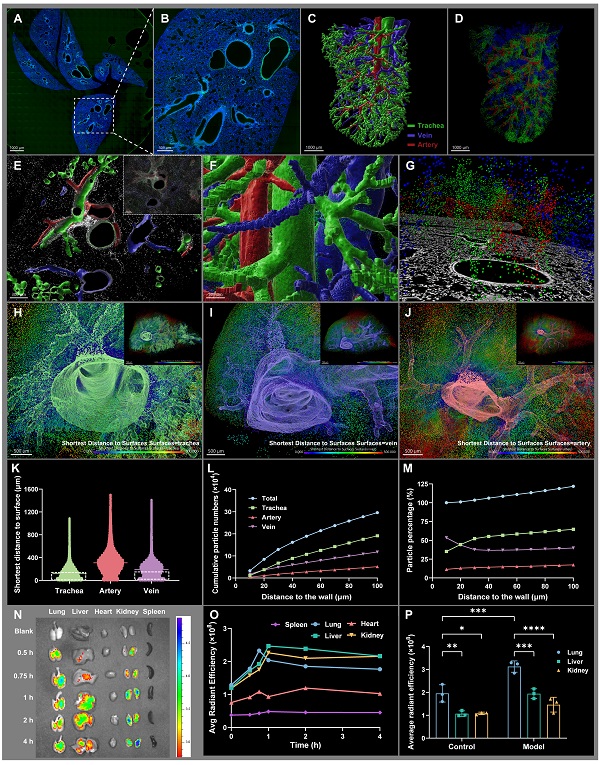
图 1 GCC-Rh110经尾静脉注射后的肺部3D空间分布:(A-B)小鼠经注射后30 min的肺部2D切片图像;(C)气管树(绿)、动脉(红)与静脉(靛蓝)的分割与3D重构;(D)GCC-Rh110粒子在气管、动脉与静脉周围的定位;(E)气管与血管系统周围区域的GCC-Rh110粒子横截面分布可视化;(F-G)管壁侧视图及其邻近区域中的粒子分布;(H-J)GCC-Rh110粒子在气管、动脉与静脉周围的最短距离定量。
该研究突破传统2D病理学的局限,基于单颗粒示踪,构建跨尺度3D定量分析体系,为肺部疾病的精准治疗及药效评估提供新策略。在脂多糖诱导的支气管炎模型中,DEX@GCC展现出显著的治疗效果,相较于DEX阳性对照组,DEX@GCC能够更快地促进体重恢复、改善肺功能,降低肺泡灌洗液中的细胞总数、蛋白浓度及炎症因子水平。此外,研究还建立了3D病理评价体系,结合机器学习识别并提取气管周围的炎性细胞,实现多级气管的虚拟内窥及气管壁厚的精准定量,进一步证实了DEX@GCC在修复气管细胞结构及缓解炎症上的优势。
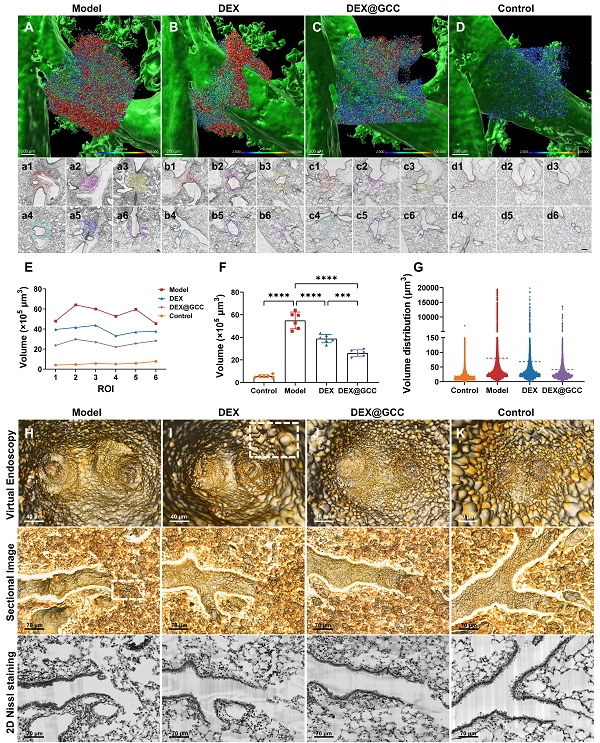
图 2 气管周围炎症细胞和肺泡上皮细胞的3D可视化:(A-D)各组ROI内细胞可视化及对应的2D Nissl切片;(E-F)各组ROI内肺泡上皮细胞和炎性细胞的体积(n=6);(G)细胞体积分布(<2×10⁴ μm³,虚线表示均值)。
在制剂科学不断向结构化与精准化发展的背景下,合作团队率先提出“结构药剂学”的新理念,创新性地引入同步辐射成像技术,精准表征制剂的结构特征,揭示结构与质量之间的关系。同时,研究团队进一步将这一理念拓展至生命组织层面,结合跨尺度3D成像,直观呈现肺部病灶的结构异质性与微环境特征,精准刻画递药系统在体内的分布规律。3D病理驱动的研究方式为纳米递药系统的设计与优化提供了坚实基础,也为个体化诊疗提供了新的思路与技术支撑。
上海药物所博士研究生曹泽颖、临港实验室科研助理周时林和赵艳丽为本文的共同第一作者;该研究由临港实验室殷宪振研究员和上海药物所张继稳研究员共同指导。上海药物所MOST及图像融合分析平台共同参与了fMOST数据的采集。该研究获得了国家自然科学基金项目和上海市东方英才计划(青年项目)的资助。该研究中的细胞实验得到了国家蛋白质科学中心(上海高等研究院)的大力支持。
原文链接:https://pubs.acs.org/doi/10.1021/acsnano.5c06694
(供稿部门:张继稳课题组、MOST及图像融合分析服务平台)