Nat Commun | 上海药物所开发超声激活型聚多肽纳米佐剂
免疫佐剂是指一类能激活特定先天免疫信号通路的物质,如Toll样受体(TLR)激动剂、干扰素刺激因子(STING)激动剂等,当其与肿瘤抗原联合使用时,能有效刺激树突细胞熟化并促进抗原交叉呈递与T细胞激活。与此同时,免疫佐剂还具有重塑肿瘤免疫抑制微环境的能力,其通过重编程M2型巨噬细胞及限制髓源性抑制细胞功能以增强细胞毒性T淋巴细胞浸润与杀伤。然而,尽管具有以上潜力,传统制剂形式的免疫佐剂在系统给药时仍然面临严重的非特异性组织分布与脱靶激活问题,从而导致剂量限制性免疫毒性产生,并阻碍其进一步临床转化与应用。
针对上述挑战,在前期工作中,中国科学院上海药物研究所于海军课题组将一系列传统小分子类免疫佐剂有效装载至纳米递送系统中以构建纳米佐剂文库。借助于纳米颗粒的被动转运特性,纳米佐剂在给药后能够高效地靶向次级淋巴器官(如引流淋巴结)而减少免疫佐剂在非靶器官(如肝脏)的分布,从而有效促进淋巴结内树突细胞抗原交叉呈递与肿瘤特异性T细胞激活(Adv Mater 2022,2209910; Nat Commun 2025,16:5773; J Am Chem Soc 2025,147:42221)。以上研究成果表明通过设计高效且安全的免疫佐剂激活策略,以提高靶器官内先天免疫反应的有效性与可控性,对于改善肿瘤免疫治疗具有重要的研究价值和科学意义。
2025年12月16日,于海军课题组在Nature Communications上发表了题为“Polypeptide Sono-Adjuvant for Ultrasound-Activatable Regulation of Innate Immunity and Cancer Vaccination Therapy”的研究论文,该研究创新性地构建了超声激活型聚多肽纳米佐剂平台,其在超声刺激条件下能够时空可控地调节淋巴结内先天免疫反应激活。同时,纳米佐剂平台可普适性高效递送肿瘤特异性新生抗原多肽,并在体内诱导强烈且特异的抗肿瘤T细胞免疫应答。这项研究成果展示了将外源物理刺激转译为精准免疫信号的治疗原型,为后续开发刺激响应型的精准免疫佐剂策略提供重要参考。
研究人员率先将临床批准使用的声敏剂(血卟啉单甲醚,HMME)共价偶联至生物可降解聚多肽骨架上以构建声敏化聚多肽,其在超声刺激条件下能够精准产生机械效应与氧化效应以协同诱导树突细胞熟化与先天免疫反应激活,即具有超声激活型免疫佐剂活性。随后,研究人员通过表面糖配体修饰与电荷修饰策略进一步筛选优化了聚多肽纳米佐剂处方,使其具备主动且高效靶向淋巴结内树突细胞的能力。相比传统TLR激动剂或STING激动剂,聚多肽纳米佐剂在联合超声刺激后(SONA + US)能够有效提高淋巴结内先天免疫反应的激活水平,同时规避系统免疫毒性即外周细胞因子风暴的产生。此外,该超声激活型免疫佐剂策略可进一步用于增强肿瘤新生抗原多肽疫苗治疗。包载有肝癌特异性新抗原多肽的纳米佐剂与超声刺激联合治疗时,能够诱导强烈且安全的抗肿瘤T细胞免疫应答,显著抑制小鼠原位肝脏肿瘤生长,并延长荷瘤小鼠生存期(图1)。
上海药物所陈方敏博士为论文第一作者,上海药物所于海军研究员和华东师范大学徐志爱教授为本文共同通讯作者。福建医科大学刘小龙教授、蔡志雄研究员对本课题给予了大力支持。该研究得到了国家重点研发计划、国家自然科学基金、中国科学院先导专项、上海市科委、国家博士后基金和生命过程小分子调控全国重点实验室等项目资助。生物效应评价部分得到了张江实验室国家蛋白质科学研究(上海)设施的大力支持。
文章链接:https://www.nature.com/articles/s41467-025-66976-2
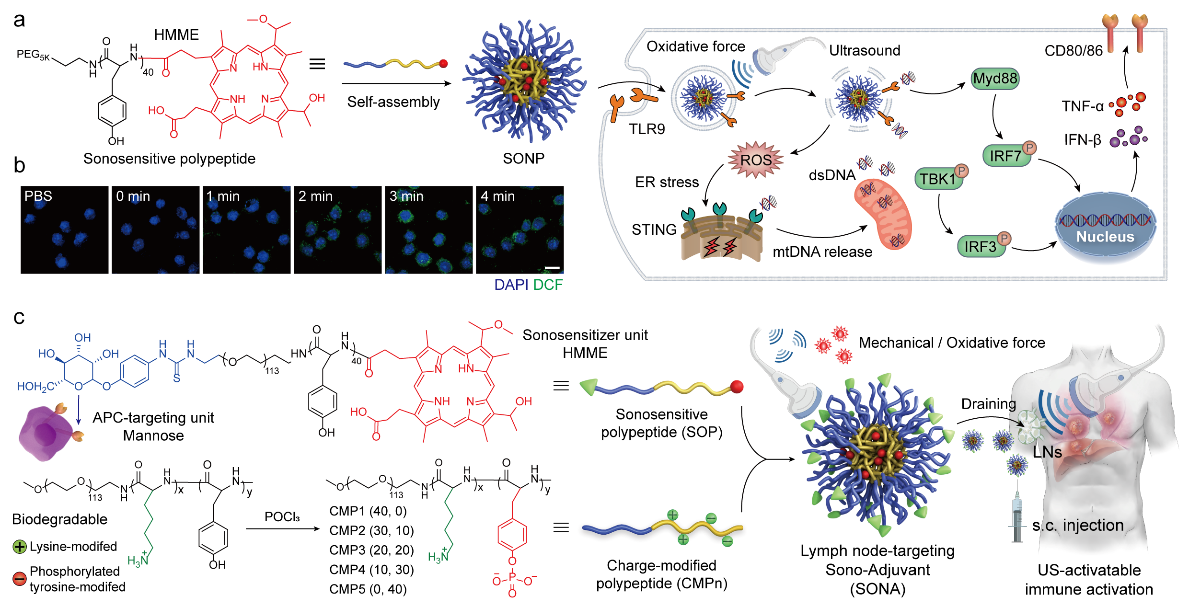
图1:超声激活型聚多肽纳米佐剂增强肿瘤新抗原疫苗治疗示意图
(供稿部门:于海军课题组)